摘要:15.已知可逆反应N2O4(g) 2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273K时,平衡常数K2=2.8×104,转化率为b%,则下列叙述正确的是: A.由于K2>K1 ,所以a>b B.由于K随温度升高而增大,所以此反应的△H>0 C.由于K随温度升高而增大,所以此反应的△H<0 D.其它条件不变时.将盛有该混合气体的容器置于热水中.体系颜色变浅
网址:http://m.1010jiajiao.com/timu3_id_282751[举报]
已知可逆反应N2O4(g) 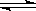 2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
| A.由于K2>K1,所以a>b |
| B.由于K随温度升高而增大,所以此反应的△H>0 |
| C.由于K随温度升高而增大,所以此反应的△H<0 |
| D.其它条件不变时,将盛有该混合气体的容器置于热水中,体系颜色变浅 |
已知可逆反应N2O4(g) 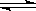 2NO2(g)
在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
2NO2(g)
在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
A.由于K2>K1,所以a>b
B.由于K随温度升高而增大,所以此反应的△H>0
C.由于K随温度升高而增大,所以此反应的△H<0
D.其它条件不变时,将盛有该混合气体的容器置于热水中,体系颜色变浅
查看习题详情和答案>>
已知可逆反应N2O4(g) 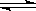 2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
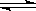 2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是| A.由于K2>K1,所以a>b |
| B.由于K随温度升高而增大,所以此反应的△H>0 |
| C.由于K随温度升高而增大,所以此反应的△H<0 |
| D.其它条件不变时,将盛有该混合气体的容器置于热水中,体系颜色变浅 |