摘要:17.某稀硝酸溶液能溶解2.7gAl.则该稀硝酸能溶解Fe的量最多是 A. 5.6g B. 8.4g C. 11.2g D. 16.8g
网址:http://m.1010jiajiao.com/timu3_id_278020[举报]
下列说法中,正确的是( )
| A、某气体能使品红溶液褪色,则该气体是SO2 | B、向某溶液中加入AgNO3溶液,产生白色沉淀,则原溶液中有Cl- | C、向某溶液中加入Ba(NO3)2溶液,产生白色沉淀,加入稀硝酸沉淀不溶解,则原溶液中有SO42- | D、向某溶液中加入NaOH并加热,产生可使湿润红色石蕊试纸变蓝的气体,则原溶液中有NH4+ |
有一包白色固体,可能含有KCl,Na2SO4,BaCl2,CuSO4和Na2CO3中的一种或几种,为探究其成分,某同学做了如下实验:
①将此白色固体取样,溶解于水,有白色沉淀生成;
②过滤出沉淀,并将沉淀移入试管中,加入稀盐酸,沉淀完全溶解并有气体生成;
③向②滤液中加入硝酸银溶液,有白色沉淀生成,再加稀硝酸沉淀不溶解.
通过上述实验现象回答以下问题:
(1)该白色固体中一定含有的物质是 (填化学式),
(2)一定不含的物质是 (填化学式),
(3)不能确定的是 (填化学式),若要确定它需要的实验方法是(填写实验名称和现象即可)
(4)写出①中发生的反应的化学反应方程式: .
查看习题详情和答案>>
①将此白色固体取样,溶解于水,有白色沉淀生成;
②过滤出沉淀,并将沉淀移入试管中,加入稀盐酸,沉淀完全溶解并有气体生成;
③向②滤液中加入硝酸银溶液,有白色沉淀生成,再加稀硝酸沉淀不溶解.
通过上述实验现象回答以下问题:
(1)该白色固体中一定含有的物质是
(2)一定不含的物质是
(3)不能确定的是
(4)写出①中发生的反应的化学反应方程式:
某学习小组设计了如图装置进行浓、稀硝酸分别与NO反应的实验,以探究浓、稀硝酸氧化性的相对强弱(夹持仪器已略去).
还可选用的药品:浓硝酸、3mol?L-1稀硝酸、蒸馏水、浓硫酸、足量氢氧化钠溶液
已知:
①浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此可得出浓硝酸的氧化性强于稀硝酸的结论.
②氢氧化钠溶液不与NO反应,但能与NO2发生反应,生成NaNO3与NaNO2
(1)加药品时,若已知③中装的是稀硝酸,为了达到探究目的,并避免实验过程有害气体排放到空气中,则还应在装置②、④、⑥中依次加入的药品是
(2)滴加浓硝酸之前,应打开弹簧夹a,通入N2一段时间,目的是
(3)写出装置①中发生反应的化学方程式
(4)装置②的作用是
(5)该小组得出探究结论所依据的实验现象是
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中可行的是(选填序号字母)
a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
查看习题详情和答案>>

还可选用的药品:浓硝酸、3mol?L-1稀硝酸、蒸馏水、浓硫酸、足量氢氧化钠溶液
已知:
①浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此可得出浓硝酸的氧化性强于稀硝酸的结论.
②氢氧化钠溶液不与NO反应,但能与NO2发生反应,生成NaNO3与NaNO2
(1)加药品时,若已知③中装的是稀硝酸,为了达到探究目的,并避免实验过程有害气体排放到空气中,则还应在装置②、④、⑥中依次加入的药品是
水
水
、浓硝酸
浓硝酸
、氢氧化钠溶液
氢氧化钠溶液
.(2)滴加浓硝酸之前,应打开弹簧夹a,通入N2一段时间,目的是
赶净装置中的空气,使整个装置充满氮气,防止装置②中反应生成的NO被空气氧化
赶净装置中的空气,使整个装置充满氮气,防止装置②中反应生成的NO被空气氧化
.关闭弹簧夹a后,还应进行的操作是将装置⑤中的导管末端伸入倒置的烧瓶内
将装置⑤中的导管末端伸入倒置的烧瓶内
,然后再打开弹簧夹b,滴加浓硝酸.(3)写出装置①中发生反应的化学方程式
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
.(4)装置②的作用是
将NO2转化为NO
将NO2转化为NO
.装置⑥的作用是2NO2+2OH-=NO3-+NO2-+H2O
2NO2+2OH-=NO3-+NO2-+H2O
(用离子方程式表示).(5)该小组得出探究结论所依据的实验现象是
装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色
装置③中液面上方气体仍为无色,装置④中液面上方气体由无色变为红棕色
.(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中可行的是(选填序号字母)
acd
acd
.a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
有一包白色固体,可能含有NaCl,Na2SO4,BaCl2和Na2CO3中的一种或几种,为探究其成分,某同学做了如下实验:
(1)将此白色固体取样,溶解于水,有白色沉淀生成;
(2)过滤出沉淀,并将沉淀移入试管中,加入稀盐酸,沉淀完全溶解并有气体生成;
(3)向上述滤液中加入硝酸银溶液,有白色沉淀生成,再加稀硝酸沉淀不溶解.
通过上述实验现象分析:该白色固体中一定含有的物质是
查看习题详情和答案>>
(1)将此白色固体取样,溶解于水,有白色沉淀生成;
(2)过滤出沉淀,并将沉淀移入试管中,加入稀盐酸,沉淀完全溶解并有气体生成;
(3)向上述滤液中加入硝酸银溶液,有白色沉淀生成,再加稀硝酸沉淀不溶解.
通过上述实验现象分析:该白色固体中一定含有的物质是
Na2CO3、BaCl2
Na2CO3、BaCl2
,一定不含的物质是Na2SO4
Na2SO4
,不能确定的是NaCl
NaCl
.某研究性学习小组,用浓硝酸、3mo/L稀硝酸、蒸馏水、氢氧化钠溶液及二氧化碳等药品,按下图装置进行试验(夹持仪器已略去),探究浓、稀硝酸氧化性的相对强弱.实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO,由此得出的结论是浓硝酸的氧化性强于稀硝酸.
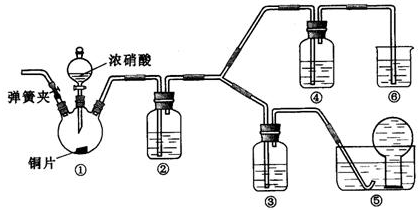
(1)装置①中发生反应的化学方程式是 .
(2)装置②的药品是水,则发生反应的化学方程式是 .
(3)装置③中盛放3mo/L稀硝酸、装置④中盛放浓硝酸,则装置④的液面上面可观察到 ;装置⑥中盛放氢氧化钠溶液,其作用是 .
(4)检验装置的气密性后,加入药品.在装置①滴加浓硝酸之前,需打开弹簧夹,通入CO2一段时间,再关闭弹簧夹,该操作目的是 .
(5)试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别设计了以下3个试验来判断两种看法是否正确.这些方案中可行的是 (选填序号字母)
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
查看习题详情和答案>>

(1)装置①中发生反应的化学方程式是
(2)装置②的药品是水,则发生反应的化学方程式是
(3)装置③中盛放3mo/L稀硝酸、装置④中盛放浓硝酸,则装置④的液面上面可观察到
(4)检验装置的气密性后,加入药品.在装置①滴加浓硝酸之前,需打开弹簧夹,通入CO2一段时间,再关闭弹簧夹,该操作目的是
(5)试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别设计了以下3个试验来判断两种看法是否正确.这些方案中可行的是
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.