网址:http://m.1010jiajiao.com/timu3_id_276564[举报]
共价键产生极性的原因是
A、 成键原子间原子吸引共用电子对能力不同
B、 成键原子由不同种原子组成
C、 成键原子由同种原子组成
D、成键原子间一种原子带部分正电荷,另一种原子带部分负电荷
查看习题详情和答案>>A. 成键原子间原子核吸收共用电子对的能力不同
B. 成键原子由同种原子组成
C. 成键原子由不同种原子组成,
D. 成键原子间一种原子带部分正电荷、一种原子带部分负电荷
查看习题详情和答案>>
共价键产生极性的根本原因是( )
A. 成键原子间原子核吸收共用电子对的能力不同
B. 成键原子由同种原子组成
C. 成键原子由不同种原子组成,
D. 成键原子间一种原子带部分正电荷、一种原子带部分负电荷
查看习题详情和答案>>
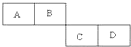 A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.
A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.(1)B在元素周期表中位于
(2)A与氢元素可以形成很多化合物,在这些化合物中都含有
(3)Na 2C溶液呈碱性,其原因是
(4)用石墨电极电解NaD溶液,阴极产物是
(5)一定温度下,在密闭容器内A的单质与水蒸气发生反应生成水煤气,水蒸气的浓度变化如下图:
反应达到平衡时的平均反应速率v=

(6)B的一种氢化物B2H4可在氧气中燃烧,可制成燃料电池,电解质溶液是KOH溶液.该电池的正极的电极反应式是
A、B、C、D、E、F均为短周期元素,且原子序数依次增大,A是原子半径最小的元素,B的最高价氧化物的水化物可与其氢化物反应形成离子化合物甲;A与D可以按照原子个数比4∶1形成化合物乙,且乙分子中含有18个电子,E与B同主族,C的阳离子与F的阴离子相差一个电子层,且可形成离子个数比为2:1的离子化合物丙。
(1)D的原子结构示意图为__________________,丙的电子式为____________________,E在周期表中的位置为_____________。
(2)下列说法正确的有__________________________
① 化合物乙为正四面体形分子,是由极性键构成的非极性分子
② C、D、E、F原子半径由大到小的顺序为 C> D >E> F
③ B、E形成的氢化物中,B的氢化物稳定性更强,是因为该分子中存在氢键
④ 化合物甲和化合物丙都含有离子键和共价键
(3)已知通常状况下1g F在空气中完全燃烧放出a kJ的热量,请写出表示F燃烧热的热化学方程式 。将燃烧产物通入BaCl2和HNO3的混合溶液,生成白色沉淀并放出无色气体,请用一个离子方程式表示该反应____________。
(4)写出一个由以上元素构成的10e-微粒与18e-微粒反应的离子方程式:
___________________________________________________________________
查看习题详情和答案>>