摘要:33.在NH4NO3的水溶液中.各离子的物质的量浓度由大到小的顺序是: c(NO3-)> c(NH4+)> c(H+) >c(OH-) . (2)溶质的物质的量浓度均为0.1mol·L-1 的下述八种溶液:①HNO3 ②KOH ③CH3COOH ④Ba(OH)2 ⑤CH3COONa ⑥H2SO4 ⑦KCl ⑧NH4Cl ⑨NH3· H2O.这些溶液的pH由小到大的顺序是 ⑥①③⑧⑦⑤⑨②④
网址:http://m.1010jiajiao.com/timu3_id_275011[举报]
已知100℃时水的离子积Kw是1.0×10-12,回答下列问题:
(1)100℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与硫酸溶液的体积比为
(2)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液中各离子浓度以它们的系数为次方的乘积是一个常数,这个常数叫溶度积(Ksp).如Cu(OH)2?Cu2++2OH-
Ksp=c(Cu2+)?c2(OH-)=2×10-20.溶液里各离子浓度(包括其方次)的乘积大于溶度积时则出现沉淀;反之则沉淀溶解.
①某CuSO4溶液里c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于
②要使0.2mol/L CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+溶液降低至原来的千分之一),则应向溶液中加入NaOH溶液,使溶液pH为
(3)25℃在等体积的①pH=0的H2SO4溶液,②0.05mol?L-1的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是
(4)在100℃时,向V mL pH=a的盐酸中滴加pH=b的NaOH溶液10V mL,所得混合溶液中c(Cl-)=c(Na+),则此时(a+b)的值为
查看习题详情和答案>>
(1)100℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与硫酸溶液的体积比为
1:9
1:9
(2)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液中各离子浓度以它们的系数为次方的乘积是一个常数,这个常数叫溶度积(Ksp).如Cu(OH)2?Cu2++2OH-
Ksp=c(Cu2+)?c2(OH-)=2×10-20.溶液里各离子浓度(包括其方次)的乘积大于溶度积时则出现沉淀;反之则沉淀溶解.
①某CuSO4溶液里c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于
5
5
.②要使0.2mol/L CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+溶液降低至原来的千分之一),则应向溶液中加入NaOH溶液,使溶液pH为
6
6
.(3)25℃在等体积的①pH=0的H2SO4溶液,②0.05mol?L-1的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是
1:10:1010:109
1:10:1010:109
(4)在100℃时,向V mL pH=a的盐酸中滴加pH=b的NaOH溶液10V mL,所得混合溶液中c(Cl-)=c(Na+),则此时(a+b)的值为
11
11
.下表为长式周期表的一部分,其中的编号代表对应的元素.
(1)写出上表中元素⑨原子的外围电子排布式
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为:
(3)元素④的第一电离能
(4)在测定①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:
(5)元素④的最高价氧化物对应的水化物稀溶液与元素⑦的单质反应时,元素④被还原到最低价,该反应的化学方程式是:
(6)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,其离子方程式为:
查看习题详情和答案>>
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |
3d54s1
3d54s1
.(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为:
sp2
sp2
杂化,元素⑦与⑧形成的化合物的晶体类型是:离子晶体
离子晶体
.(3)元素④的第一电离能
>
>
元素⑤(选填“>”、“=”、“<”)的第一电离能;元素④与元素①形成的X分子的空间构型为:三角锥型
三角锥型
.请写出与N2互为等电子体的分子、离子的化学式CO
CO
、C22-
C22-
(各写一种).(4)在测定①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:
HF分子间形成氢键
HF分子间形成氢键
.(5)元素④的最高价氧化物对应的水化物稀溶液与元素⑦的单质反应时,元素④被还原到最低价,该反应的化学方程式是:
4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
.(6)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,其离子方程式为:
Cu2++4NH3=[Cu(NH3)4]2+
Cu2++4NH3=[Cu(NH3)4]2+
.(13分)
(1) 用NH3做主要原料按下列流程生产化肥NH4NO3。其中a%、b%、c%分别表示对应反应的转化率,NH3与HNO3反应生成NH4NO3原料利用率为100%
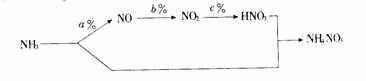
若用1tNH3为原料,为了使制得的NH4NO3产量最大,则用于制HNO3的NH3质量为 t(用含a、b、c的代数式表示)
(2) 铵态氮肥在碱性条件下使用会导致肥效损失,NH4H2PO4溶液与足量NaOH溶液共热反应的离子方程式为 。
(3) 一种复合肥料含有NH4NO3 、NH4H2PO4、KCl,取其一定量溶于水形成溶液,测得其中部分离子浓度为:c(NH4+)=3mol•l-1,c(H2PO4-)=2mol•l-1,c(K+)=2mol•l-1,则配制该复合肥料所取的NH4NO3 、NH4H2PO4、KCl的物质的量之比为 。
(4) 人们一直致力于人工固氮的研究以获得廉价的氮肥。科学家先后提出并合成固氮酶的多种模拟物。其中一类是含Mo、Fe、S原子的“类立方体”结构,如图所示:
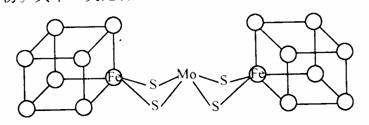
图中左、右两边对称,各含一个近似为立方体的结构。每个立方体含有4个Fe原子、4个S原子,它们位于立方体的8个顶点,且原子间只有一种化学键。
①请在图中左边立方体的○中填写出其余3个Fe原子。
②上述一个立方体中4个Fe原子所在的顶点连接所构成的空间几何体为 。
查看习题详情和答案>>(附加题)A、B、C、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子化合物;B与Z的最外层电子数之比为2:3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红.
请回答下列问题:
(1)Z的原子结构示意图为
 ;元素C在周期表中的位
;元素C在周期表中的位
置是
 ;
;
(2)化合物Y2X2属于离子化合物,含有的化学键是
(3)化合物A2X和A2Z中,沸点较高的是
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物反应可以生成Z单质和一种10电子化合物,反应的化学方程式为
(5)用电子式表示化合物Y2X的形成过程

(6)已知X2和ZX2合成ZX3的化学方程式为:2ZX2(g)+X2(g) 2ZX3(g),在一定温度下的定容容器中,下列事实不能说明该反应已经达到平衡的标志的是
2ZX3(g),在一定温度下的定容容器中,下列事实不能说明该反应已经达到平衡的标志的是
A.ZX3的生成速率与ZX3的分解速率相等
B.单位时间内生成1mol X2,同时生成2mol ZX2
C.容器内ZX2、X2、ZX3的浓度之比为2:1:2
D.容器中各组分的含量不在随时间变化而变化
E.容器中气体的压强不在随时间变化而变化
(7)写出元素C的最高价氧化物对应水化物与元素C的气态氢化物反应的化学方程式
查看习题详情和答案>>
请回答下列问题:
(1)Z的原子结构示意图为


置是
第二周期ⅤA
第二周期ⅤA
,A与B所形成的化合物BA4的电子式为

(2)化合物Y2X2属于离子化合物,含有的化学键是
离子键和非极性键
离子键和非极性键
,该化合物中阳离子与阴离子的个数比为2:1
2:1
;(3)化合物A2X和A2Z中,沸点较高的是
H2O
H2O
(填化学式);(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物反应可以生成Z单质和一种10电子化合物,反应的化学方程式为
H2O2+H2S=S↓+2H2O
H2O2+H2S=S↓+2H2O
删除此空
删除此空
;(5)用电子式表示化合物Y2X的形成过程


删除此空
删除此空
;(6)已知X2和ZX2合成ZX3的化学方程式为:2ZX2(g)+X2(g)
 2ZX3(g),在一定温度下的定容容器中,下列事实不能说明该反应已经达到平衡的标志的是
2ZX3(g),在一定温度下的定容容器中,下列事实不能说明该反应已经达到平衡的标志的是BC
BC
;A.ZX3的生成速率与ZX3的分解速率相等
B.单位时间内生成1mol X2,同时生成2mol ZX2
C.容器内ZX2、X2、ZX3的浓度之比为2:1:2
D.容器中各组分的含量不在随时间变化而变化
E.容器中气体的压强不在随时间变化而变化
(7)写出元素C的最高价氧化物对应水化物与元素C的气态氢化物反应的化学方程式
HNO3+NH3=NH4NO3
HNO3+NH3=NH4NO3
.已知100℃时水的离子积Kw是1.0×10-12,回答下列问题:
(1)100℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与硫酸溶液的体积比为______
(2)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液中各离子浓度以它们的系数为次方的乘积是一个常数,这个常数叫溶度积(Ksp).如Cu(OH)2?Cu2++2OH-
Ksp=c(Cu2+)?c2(OH-)=2×10-20.溶液里各离子浓度(包括其方次)的乘积大于溶度积时则出现沉淀;反之则沉淀溶解.
①某CuSO4溶液里c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于______.
②要使0.2mol/L CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+溶液降低至原来的千分之一),则应向溶液中加入NaOH溶液,使溶液pH为______.
(3)25℃在等体积的①pH=0的H2SO4溶液,②0.05mol?L-1的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是______
(4)在100℃时,向V mL pH=a的盐酸中滴加pH=b的NaOH溶液10V mL,所得混合溶液中c(Cl-)=c(Na+),则此时(a+b)的值为______.
查看习题详情和答案>>
(1)100℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与硫酸溶液的体积比为______
(2)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液中各离子浓度以它们的系数为次方的乘积是一个常数,这个常数叫溶度积(Ksp).如Cu(OH)2?Cu2++2OH-
Ksp=c(Cu2+)?c2(OH-)=2×10-20.溶液里各离子浓度(包括其方次)的乘积大于溶度积时则出现沉淀;反之则沉淀溶解.
①某CuSO4溶液里c(Cu2+)=0.02mol/L,如果要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于______.
②要使0.2mol/L CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+溶液降低至原来的千分之一),则应向溶液中加入NaOH溶液,使溶液pH为______.
(3)25℃在等体积的①pH=0的H2SO4溶液,②0.05mol?L-1的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是______
(4)在100℃时,向V mL pH=a的盐酸中滴加pH=b的NaOH溶液10V mL,所得混合溶液中c(Cl-)=c(Na+),则此时(a+b)的值为______.