摘要:一化工厂排放的废液 中行有少量的Na2CO3.为测定Na2CO3 的质量分数.某化学兴趣小组同学 取该废液200g予一烧杯中.然后往 里面滴入稀盐酸.所滴入稀盐酸的质 量与产生气体的体积关系曲线如图所 示.(已知:CO2密度为2g/L) 求: (1)A点时烧杯中溶液里的溶质是 ,C点时烧杯中溶液里的溶质是 (2)废液中Na2CO3的质量分数
网址:http://m.1010jiajiao.com/timu3_id_12949[举报]
某工厂排放的废水中含有大量的硫酸亚铁,少量的银离子以及污泥.某校兴趣小组的同学设计了一个既经济又合理的方法回收银和硫酸亚铁晶体.方案流程如下:

回答下列问题:
(1)步骤②中:需加入过量的物质是______,溶液2的溶质是______.
(2)步骤③中:需加入适量的物质是______(填化学式),发生反应的化学方程式是______,该反应属于______反应(选填“化合”、“分解”、“置换”或“复分解”).
(3)某同学认为经过步骤②后所得固体就是纯净的银,不需要进行步骤③,你认为是否合理?______,理由是______.
查看习题详情和答案>>
某工厂排放的废水中含有大量的硫酸亚铁,少量的银离子以及污泥.某校兴趣小组的同学设计了一个既经济又合理的方法回收银和硫酸亚铁晶体.方案流程如下:
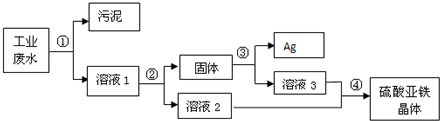
回答下列问题:
(1)步骤②中:需加入过量的物质是______,溶液2的溶质是______.
(2)步骤③中:需加入适量的物质是______(填化学式),发生反应的化学方程式是______,该反应属于______反应(选填“化合”、“分解”、“置换”或“复分解”).
(3)某同学认为经过步骤②后所得固体就是纯净的银,不需要进行步骤③,你认为是否合理?______,理由是______.
查看习题详情和答案>>

回答下列问题:
(1)步骤②中:需加入过量的物质是______,溶液2的溶质是______.
(2)步骤③中:需加入适量的物质是______(填化学式),发生反应的化学方程式是______,该反应属于______反应(选填“化合”、“分解”、“置换”或“复分解”).
(3)某同学认为经过步骤②后所得固体就是纯净的银,不需要进行步骤③,你认为是否合理?______,理由是______.
某工厂排放的废水中含有大量的硫酸亚铁,少量的银离子以及污泥.某校兴趣小组的同学设计了一个既经济又合理的方法回收银和硫酸亚铁晶体.方案流程如下:
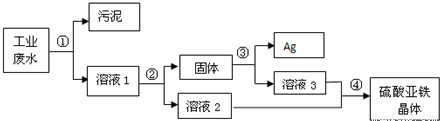
回答下列问题:
(1)步骤②中:需加入过量的物质是 ,溶液2的溶质是 .
(2)步骤③中:需加入适量的物质是 (填化学式),发生反应的化学方程式是 ,该反应属于 反应(选填“化合”、“分解”、“置换”或“复分解”).
(3)某同学认为经过步骤②后所得固体就是纯净的银,不需要进行步骤③,你认为是否合理? ,理由是 . 查看习题详情和答案>>

回答下列问题:
(1)步骤②中:需加入过量的物质是 ,溶液2的溶质是 .
(2)步骤③中:需加入适量的物质是 (填化学式),发生反应的化学方程式是 ,该反应属于 反应(选填“化合”、“分解”、“置换”或“复分解”).
(3)某同学认为经过步骤②后所得固体就是纯净的银,不需要进行步骤③,你认为是否合理? ,理由是 . 查看习题详情和答案>>
对生活中常见金属的有关问题探究:
人类从石器时代进入青铜器时代,继而进入铁器时代;前两个世纪中钢铁产量是衡量国家工业和经济发展的标志.可见金属材料长期以来一直被广泛地应用着.对金属材料的探究要用到许多化学知识.
(1)“金属之最”:完成(1)~(2)的空格,并以此为例,再另外写出两个“金属之最”.
①目前世界上年产量最高的金属是
②地壳中含量最多的金属是
③
(2)“变废为宝,回收利用”:某厂的废液中含有H2SO4和CuSO4,为了防止废酸和CuSO4污染环境,厂家设计用含铁的废弃物回收金属铜,同时生产重要的化工原料硫酸亚铁晶体,设计原理如图所示:
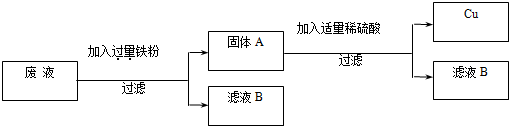
请你根据上述设计方案写出有关化学方程式: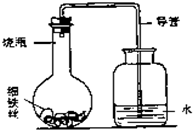
(3)“锈蚀条件的探究”:某学生在A、B、C、D四只小烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝,并使铁丝完全浸没在食盐水中,然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如下表(表中所列数据为导管中水面上升的高度/cm)所示.
①导管中水面为什么会上升?
②上述实验中,铁生锈的速率由大到小的排列顺序为(填小烧瓶号):
③影响铁生锈的因素有:
(4)“金属的防护”:对如何防止你的自行车的钢圈生锈提出两种方案.
(5)“金属的冶炼”:某钢铁厂日产含4%杂质的生铁2240吨.问:需要含Fe2O3质量分数为80%的赤铁矿石多少吨?
查看习题详情和答案>>
人类从石器时代进入青铜器时代,继而进入铁器时代;前两个世纪中钢铁产量是衡量国家工业和经济发展的标志.可见金属材料长期以来一直被广泛地应用着.对金属材料的探究要用到许多化学知识.
(1)“金属之最”:完成(1)~(2)的空格,并以此为例,再另外写出两个“金属之最”.
①目前世界上年产量最高的金属是
铁
铁
;②地壳中含量最多的金属是
铝
铝
;③
熔点最低的金属是汞
熔点最低的金属是汞
;④熔点最高的金属是钨
熔点最高的金属是钨
.(2)“变废为宝,回收利用”:某厂的废液中含有H2SO4和CuSO4,为了防止废酸和CuSO4污染环境,厂家设计用含铁的废弃物回收金属铜,同时生产重要的化工原料硫酸亚铁晶体,设计原理如图所示:

请你根据上述设计方案写出有关化学方程式:
Fe+H2SO4 ═FeSO4+H2↑
Fe+H2SO4 ═FeSO4+H2↑
;Fe+CuSO4═Cu+FeSO4
Fe+CuSO4═Cu+FeSO4
.
(3)“锈蚀条件的探究”:某学生在A、B、C、D四只小烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝,并使铁丝完全浸没在食盐水中,然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如下表(表中所列数据为导管中水面上升的高度/cm)所示.
| 时间/小时 | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A瓶(盛干燥铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B瓶(盛沾了食盐水的铁丝) | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
| C瓶(盛沾了清水的铁丝) | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| D瓶(盛完全浸没在食盐水中的铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
铁生锈时消耗氧气,使瓶内压强降低
铁生锈时消耗氧气,使瓶内压强降低
.②上述实验中,铁生锈的速率由大到小的排列顺序为(填小烧瓶号):
B>C>A=D
B>C>A=D
.③影响铁生锈的因素有:
水和氧气,有盐溶液速度最快.
水和氧气,有盐溶液速度最快.
.(4)“金属的防护”:对如何防止你的自行车的钢圈生锈提出两种方案.
镀一层金属或涂油
镀一层金属或涂油
.(5)“金属的冶炼”:某钢铁厂日产含4%杂质的生铁2240吨.问:需要含Fe2O3质量分数为80%的赤铁矿石多少吨?
 对生活中常见金属的有关问题探究:
对生活中常见金属的有关问题探究:
人类从石器时代进入青铜器时代,继而进入铁器时代;前两个世纪中钢铁产量是衡量国家工业和经济发展的标志.可见金属材料长期以来一直被广泛地应用着.对金属材料的探究要用到许多化学知识.
(1)“金属之最”:完成(1)~(2)的空格,并以此为例,再另外写出两个“金属之最”.
①目前世界上年产量最高的金属是______;
②地壳中含量最多的金属是______;
③______;④______.
(2)“变废为宝,回收利用”:某厂的废液中含有H2SO4和CuSO4,为了防止废酸和CuSO4污染环境,厂家设计用含铁的废弃物回收金属铜,同时生产重要的化工原料硫酸亚铁晶体,设计原理如图所示:
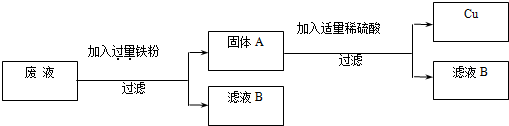
请你根据上述设计方案写出有关化学方程式:______;______.
(3)“锈蚀条件的探究”:某学生在A、B、C、D四只小烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝,并使铁丝完全浸没在食盐水中,然后装配成如图所示的四套装置,每隔一段时间测量导管中水面上升的高度,结果如下表(表中所列数据为导管中水面上升的高度/cm)所示.
| 时间/小时 | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A瓶(盛干燥铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B瓶(盛沾了食盐水的铁丝) | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
| C瓶(盛沾了清水的铁丝) | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| D瓶(盛完全浸没在食盐水中的铁丝) | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
②上述实验中,铁生锈的速率由大到小的排列顺序为(填小烧瓶号):______.
③影响铁生锈的因素有:______.
(4)“金属的防护”:对如何防止你的自行车的钢圈生锈提出两种方案.______.
(5)“金属的冶炼”:某钢铁厂日产含4%杂质的生铁2240吨.问:需要含Fe2O3质量分数为80%的赤铁矿石多少吨? 查看习题详情和答案>>