摘要:14.标准状况下.向3mol·L-1的NaOH溶液100mL中缓缓通入4.48L CO2气体.充分反应后溶液中离子浓度大小排列顺序正确的是( ) A.c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) B.c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) C.c(Na+)>c(HCO3-)>c(OH-)>c(CO32-)>c(H+) D.c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
网址:http://m.1010jiajiao.com/timu3_id_1212751[举报]
标准状况下,向100mL 3mol?L-1的NaOH溶液中缓缓通入4.48L CO2 气体,充分反应后溶液中离子浓度大小排列顺序正确的是( )
查看习题详情和答案>>
A.c(Na+)>c(CO
| ||||
B.c(Na+)>c(CO
| ||||
C.c(Na+)>c(HCO
| ||||
D.c(Na+)>c(HCO
|
标准状况下,向100mL 3mol?L-1的NaOH溶液中缓缓通入4.48L CO2 气体,充分反应后溶液中离子浓度大小排列顺序正确的是( )
A.c(Na+)>c(CO )>c(HCO
)>c(HCO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.c(Na+)>c(CO )=c(HCO
)=c(HCO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
C.c(Na+)>c(HCO )>c(OH-)>c(CO
)>c(OH-)>c(CO )>c(H+)
)>c(H+)
D.c(Na+)>c(HCO )>c(CO
)>c(CO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
查看习题详情和答案>>
A.c(Na+)>c(CO
 )>c(HCO
)>c(HCO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)B.c(Na+)>c(CO
 )=c(HCO
)=c(HCO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)C.c(Na+)>c(HCO
 )>c(OH-)>c(CO
)>c(OH-)>c(CO )>c(H+)
)>c(H+)D.c(Na+)>c(HCO
 )>c(CO
)>c(CO )>c(OH-)>c(H+)
)>c(OH-)>c(H+)查看习题详情和答案>>
下列说法正确的是
- A.把NaHCO3和Na2CO3混和物6.85g溶于水制成100mL溶液,其中c(Na+)=1mol?L-1.该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量无法计算
- B.将54.4g铁粉和氧化铁的混合物中加入4.0mol/L 200mL的稀硫酸,恰好完全反应,放出氢气4.48L(标准状况).反应后的溶液中滴加KSCN不显红色,且无固体剩余物,反应后得到FeSO4的物质的量是0.8mol
- C.现向一密闭容器中充入1mol N2和3mol H2,在一定条件下使该反应发生,达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
- D.
 某溶液中可能含有H+、Na+、
某溶液中可能含有H+、Na+、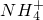 、Mg2+、Fe3+、Al3+、
、Mg2+、Fe3+、Al3+、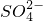 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是H+、
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是H+、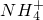 、Mg2+、Al3+
、Mg2+、Al3+
按要求回答下列问题:
(1)实验室中常用NaOH溶液来进行洗气和提纯,当100mL 3mol/L的NaOH溶液吸收标准状况下4.48L CO2时,所得溶液中各离子浓度由大到小的顺序为
(2)常温下向一定体积的0.1 mol/L醋酸溶液中加水稀释后,下列说法正确的是 。
A.溶液中导电粒子的数目减少
B醋酸的电离程度增大,c(H+)亦增大
C.溶液中 不变
不变
D溶液中 减小
减小
(3)①常温下将0.15 mol/L稀硫酸V1 mL与0.1 mol/L NaOH溶液V2 mL混合,所得溶液的pH为1,则V1:V2= (溶液体积变化忽略不计)。
②常温下若溶液由pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是
A.若反应后溶液呈中性,则
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
(4)常温下,浓度均为0.lmol/L的下列五种溶液的PH值如表所示:

①根据表中数据,将浓度均为0.01 mol/L的下列四种酸的溶液分别稀释100倍,pH变化最小的是
A.HCN B.HClO C.H2CO3 D.CH3COOH
②根据以上数据,判断下列反应可以成立的是 。

(5)几种离子开始沉淀时的pH如下表:

当向含相同浓度 离子的溶液中滴加NaOH溶液时,
(填离子符号)先沉淀,
离子的溶液中滴加NaOH溶液时,
(填离子符号)先沉淀, (填“>”、“二”或“<”)。
(填“>”、“二”或“<”)。
查看习题详情和答案>>