摘要:1.高温可使淀粉等大分子变性.便于酶的催化 淀粉酶和麦芽糖酶 淀粉→麦芽糖→葡萄糖
网址:http://m.1010jiajiao.com/timu3_id_1210749[举报]
人类发展的历史进程中人们不断研制出各种不同的用具,制造用具的材料也在不断地发生变化,金属制品因其美观、耐用、轻便易成型而被人们广泛利用,请根据所学知识及生活知识参与有关金属制品探究.
(1)以下工具的制作过程中没有发生化学变化的是(________)
A.原始人制作石刀;B.冶炼青铜;C.炼铁
(2)请将以下金属材料的冶炼按年代的先后顺序排序________(填序号).
A.铁;B.青铜;C.铝
从以上顺序可以看出,金属制品的出现顺序与________有关,那么金属钾的制得应排在
________之后.
(3)金属区别于非金属的主要物理性质是,金属具有________,金属区别于非金属的主要化学特征是在化学变化中金属原子通常表现为________.
(4)孔雀石主要成分为碱式碳酸铜,经加热会发生反应:Cu2(OH)2CO3 2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:________
2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:________
(5)古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼石成金”.
①请你用学过的知识回答,真的可以“炼石成金”吗?
________.
②那么你认为这金光灿灿的金属是什么?它是怎么炼出来的?写出有关化学方程式
该金属可能是________,炼出它的化学方程式为________、________、________.
(6)到西汉时期我国的劳动人民又发明了“湿法炼铜”,在西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载(“曾青”是指铜的化合物),请用反应方程式表示其冶炼原理:________
(7)磁悬浮的核心技术得制备超导材料.有一种超导材料的化学式为Y2BaCu6O10,它是以YmOn、BaCO3和CuO为原料经研磨烧结而成.假设此过程中所有元素的化合价不变,试填写以下空白:
a.超导材料Y2BaCu6O10是由________种元素组成的,YmOn的化学式是:________
b.在合成该超导材料的同时还生成-种产物,该物质是________(写化学式).
金属的使用及冶炼历史也引起同学们极大兴趣,初三同学组织化学兴趣小组继续进行(8)(9)探究:
(8)首先他们收集大量有关钢铁的成语与民间谚语.其中有说明钢的性能比铁好的有________,知道“百炼成钢”是指铁在高温条件下反复敲打发生的反应是:________,从而了解钢与铁的机械性能不同是因为两者________.
(9)钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究.
[提出假设]a. Ti的金属活动性比Mg强;
b.Ti的金属活动性介于Mg和Ag之间.
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属活动性越强.
[实验设计]同温下,取大小相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
请回答:三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是________.
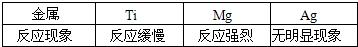
[实验现象]
| 金属 | Ti | Mg | Ag |
| 反应现象 | 反应缓慢 | 反应强烈 | 无明显现象 |
[结论]用不同浓度的足量稀盐酸反应,是否也能得出同样结论?________,请说明理由________
(10)小刚与小红分别做相同质量的不同金属与同质量、同质量分数的稀H2SO4反应的实验,实验
结束后,分别交上的实验报告,并绘制出金属Zn、Fe分别与稀H2SO4反应放出H2的函数图象(如图所示).
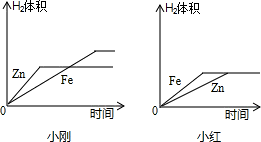
两个图象中存在有错误的是________的图象,判断错误的理由是________,
图象不同的原因是________.
由该实验可以得到的结论:
①金属与酸反应的速率与________有关.
②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与________有关.
(11)将铁粉加到一定量的硝酸银、硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,在滤液中滴加盐酸,没有白色沉淀生成,则滤渣中一定有________,肯定滤液中有________.
(12)现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一
种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn一119,Ni一59.
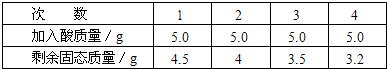
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入酸质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
| 剩余固态质量/g | 4.5 | 4 | 3.5 | 3.2 |
人类发展的历史进程中人们不断研制出各种不同的用具,制造用具的材料也在不断地发生变化,金属制品因其美观、耐用、轻便易成型而被人们广泛利用,请根据所学知识及生活知识参与有关金属制品探究.
(1)以下工具的制作过程中没有发生化学变化的是 _________
A.原始人制作石刀;B.冶炼青铜;C.炼铁
(2)请将以下金属材料的冶炼按年代的先后顺序排序_________(填序号).
A.铁;B.青铜;C.铝
从以上顺序可以看出,金属制品的出现顺序与_________,那么金属钾的制得应排在
_________.
(3)金属区别于非金属的主要物理性质是,金属具有_________,金属区别于非金属的主要化学特征是在化学变化中金属原子通常表现为_________.
(4)孔雀石主要成分为碱式碳酸铜,经加热会发生反应:Cu2(OH)2CO3 2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:_________
2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:_________
(5)古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼石成金”.
①请你用学过的知识回答,真的可以“炼石成金”吗?
_________.
②那么你认为这金光灿灿的金属是什么?它是怎么炼出来的?写出有关化学方程式
该金属可能是_________,炼出它的化学方程式为_________、_________、_________.
(6)到西汉时期我国的劳动人民又发明了“湿法炼铜”,在西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载(“曾青”是指铜的化合物),请用反应方程式表示其冶炼原理:_________
(7)磁悬浮的核心技术得制备超导材料.有一种超导材料的化学式为Y2BaCu6O10,它是以YmOn、BaCO3和CuO为原料经研磨烧结而成.假设此过程中所有元素的化合价不变,试填写以下空白:
a.超导材料Y2BaCu6O10是由_________,YmOn的化学式是:_________
b.在合成该超导材料的同时还生成一种产物,该物质是_________(写化学式).
金属的使用及冶炼历史也引起同学们极大兴趣,初三同学组织化学兴趣小组继续进行(8)(9)探究:
(8)首先他们收集大量有关钢铁的成语与民间谚语.其中有说明钢的性能比铁好的有_________,知道“百炼成钢”是指铁在高温条件下反复敲打发生的反应是:_________,从而了解钢与铁的机械性能不同是因为两者_________.
(9)钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究.
[提出假设]
a. Ti的金属活动性比Mg强;
b.Ti的金属活动性介于Mg和Ag之间.
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属活动性越强.
[实验设计]同温下,取大小相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
请回答:三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是_________.
[实验现象]
(1)以下工具的制作过程中没有发生化学变化的是 _________
A.原始人制作石刀;B.冶炼青铜;C.炼铁
(2)请将以下金属材料的冶炼按年代的先后顺序排序_________(填序号).
A.铁;B.青铜;C.铝
从以上顺序可以看出,金属制品的出现顺序与_________,那么金属钾的制得应排在
_________.
(3)金属区别于非金属的主要物理性质是,金属具有_________,金属区别于非金属的主要化学特征是在化学变化中金属原子通常表现为_________.
(4)孔雀石主要成分为碱式碳酸铜,经加热会发生反应:Cu2(OH)2CO3
 2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:_________
2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:_________(5)古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼石成金”.
①请你用学过的知识回答,真的可以“炼石成金”吗?
_________.
②那么你认为这金光灿灿的金属是什么?它是怎么炼出来的?写出有关化学方程式
该金属可能是_________,炼出它的化学方程式为_________、_________、_________.
(6)到西汉时期我国的劳动人民又发明了“湿法炼铜”,在西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载(“曾青”是指铜的化合物),请用反应方程式表示其冶炼原理:_________
(7)磁悬浮的核心技术得制备超导材料.有一种超导材料的化学式为Y2BaCu6O10,它是以YmOn、BaCO3和CuO为原料经研磨烧结而成.假设此过程中所有元素的化合价不变,试填写以下空白:
a.超导材料Y2BaCu6O10是由_________,YmOn的化学式是:_________
b.在合成该超导材料的同时还生成一种产物,该物质是_________(写化学式).
金属的使用及冶炼历史也引起同学们极大兴趣,初三同学组织化学兴趣小组继续进行(8)(9)探究:
(8)首先他们收集大量有关钢铁的成语与民间谚语.其中有说明钢的性能比铁好的有_________,知道“百炼成钢”是指铁在高温条件下反复敲打发生的反应是:_________,从而了解钢与铁的机械性能不同是因为两者_________.
(9)钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究.
[提出假设]
a. Ti的金属活动性比Mg强;
b.Ti的金属活动性介于Mg和Ag之间.
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属活动性越强.
[实验设计]同温下,取大小相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
请回答:三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是_________.
[实验现象]

[实验结论]原假设中_________不正确,理由是_________.
[结论]用不同浓度的足量稀盐酸反应,是否也能得出同样结论?_________,请说明理由_________
(10)小刚与小红分别做相同质量的不同金属与同质量、同质量分数的稀H2SO4反应的实验,实验结束后,分别交上的实验报告,并绘制出金属Zn、Fe分别与稀H2SO4反应放出H2的函数图象(如图所示).
[结论]用不同浓度的足量稀盐酸反应,是否也能得出同样结论?_________,请说明理由_________
(10)小刚与小红分别做相同质量的不同金属与同质量、同质量分数的稀H2SO4反应的实验,实验结束后,分别交上的实验报告,并绘制出金属Zn、Fe分别与稀H2SO4反应放出H2的函数图象(如图所示).

两个图象中存在有错误的是 _________ 的图象,判断错误的理由是 _________ ,
图象不同的原因是 _________ .
由该实验可以得到的结论:
①金属与酸反应的速率与 _________ 有关.
②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与 _________ 有关.
(11)将铁粉加到一定量的硝酸银、硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,在滤液中滴加盐酸,没有白色沉淀生成,则滤渣中一定有 _________ ,肯定滤液中有 _________ .
(12)现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一
种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn--65,Sn--119,Ni--59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
图象不同的原因是 _________ .
由该实验可以得到的结论:
①金属与酸反应的速率与 _________ 有关.
②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与 _________ 有关.
(11)将铁粉加到一定量的硝酸银、硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,在滤液中滴加盐酸,没有白色沉淀生成,则滤渣中一定有 _________ ,肯定滤液中有 _________ .
(12)现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一
种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn--65,Sn--119,Ni--59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:

试求:①合金中铜的质量分数_________.
②合金中另一金属为何种金属_________.
查看习题详情和答案>>
②合金中另一金属为何种金属_________.
23、人类发展的历史进程中人们不断研制出各种不同的用具,制造用具的材料也在不断地发生变化,金属制品因其美观、耐用、轻便易成型而被人们广泛利用,请根据所学知识及生活知识参与有关金属制品探究.
(1)以下工具的制作过程中没有发生化学变化的是(
A.原始人制作石刀;B.冶炼青铜;C.炼铁
(2)请将以下金属材料的冶炼按年代的先后顺序排序
A.铁;B.青铜;C.铝
从以上顺序可以看出,金属制品的出现顺序与
(3)金属区别于非金属的主要物理性质是,金属具有
(4)孔雀石主要成分为碱式碳酸铜,经加热会发生反应:Cu2(OH)2CO3△2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:
(5)古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼石成金”.
①请你用学过的知识回答,真的可以“炼石成金”吗?
②那么你认为这金光灿灿的金属是什么?它是怎么炼出来的?写出有关化学方程式
该金属可能是
(6)到西汉时期我国的劳动人民又发明了“湿法炼铜”,在西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载(“曾青”是指铜的化合物),请用反应方程式表示其冶炼原理:
(7)磁悬浮的核心技术得制备超导材料.有一种超导材料的化学式为Y2BaCu6O10,它是以YmOn、BaCO3和CuO为原料经研磨烧结而成.假设此过程中所有元素的化合价不变,试填写以下空白:
a.超导材料Y2BaCu6O10是由
b.在合成该超导材料的同时还生成-种产物,该物质是
金属的使用及冶炼历史也引起同学们极大兴趣,初三同学组织化学兴趣小组继续进行(8)(9)探究:
(8)首先他们收集大量有关钢铁的成语与民间谚语.其中有说明钢的性能比铁好的有
(9)钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究.
[提出假设]a. Ti的金属活动性比Mg强;
b.Ti的金属活动性介于Mg和Ag之间.
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属活动性越强.
[实验设计]同温下,取大小相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
请回答:三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是
[实验现象]
[实验结论]原假设中
[结论]用不同浓度的足量稀盐酸反应,是否也能得出同样结论?
(10)小刚与小红分别做相同质量的不同金属与同质量、同质量分数的稀H2SO4反应的实验,实验
结束后,分别交上的实验报告,并绘制出金属Zn、Fe分别与稀H2SO4反应放出H2的函数图象(如图所示).
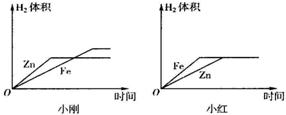
两个图象中存在有错误的是
图象不同的原因是
由该实验可以得到的结论:
①金属与酸反应的速率与
②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与
(11)将铁粉加到一定量的硝酸银、硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,在滤液中滴加盐酸,没有白色沉淀生成,则滤渣中一定有
(12)现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一
种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn一119,Ni一59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:
试求:①合金中铜的质量分数
查看习题详情和答案>>
(1)以下工具的制作过程中没有发生化学变化的是(
A
)A.原始人制作石刀;B.冶炼青铜;C.炼铁
(2)请将以下金属材料的冶炼按年代的先后顺序排序
B.A.C
(填序号).A.铁;B.青铜;C.铝
从以上顺序可以看出,金属制品的出现顺序与
金属活动性
有关,那么金属钾的制得应排在C
之后.(3)金属区别于非金属的主要物理性质是,金属具有
金属光泽
,金属区别于非金属的主要化学特征是良好的传热导电性
.在化学变化中金属原子通常表现为延展性易失去电子
.(4)孔雀石主要成分为碱式碳酸铜,经加热会发生反应:Cu2(OH)2CO3△2CuO+H2O+CO2↑,古代人们发现翠绿的孔雀石在森林大火中会变成红色的铜,请写出转化为铜的另一个反应方程式:
2CuO+2C═2Cu+CO2↑
(5)古代术士将炉甘石(主要成分为ZnCO3)与赤铜矿(Cu2O)、木炭放在炼炉中高温灼烧,炼出金光灿灿的“黄金”,被称为“炼石成金”.
①请你用学过的知识回答,真的可以“炼石成金”吗?
不能,在化学变化过程中元素种类不可能发生改变
.②那么你认为这金光灿灿的金属是什么?它是怎么炼出来的?写出有关化学方程式
该金属可能是
铜锌合金
,炼出它的化学方程式为ZnCO3═ZnO+CO2↑
、2ZnO+C═2Zn+CO2↑
、2Cu2O+C═4Cu+CO2↑
.(6)到西汉时期我国的劳动人民又发明了“湿法炼铜”,在西汉刘安所著的《淮南万毕术》中就有“曾青得铁则化为铜”的记载(“曾青”是指铜的化合物),请用反应方程式表示其冶炼原理:
Fe+CuSO4═Cu+FeSO4
(7)磁悬浮的核心技术得制备超导材料.有一种超导材料的化学式为Y2BaCu6O10,它是以YmOn、BaCO3和CuO为原料经研磨烧结而成.假设此过程中所有元素的化合价不变,试填写以下空白:
a.超导材料Y2BaCu6O10是由
四
种元素组成的,YmOn的化学式是:Y2O3
b.在合成该超导材料的同时还生成-种产物,该物质是
CO2
(写化学式).金属的使用及冶炼历史也引起同学们极大兴趣,初三同学组织化学兴趣小组继续进行(8)(9)探究:
(8)首先他们收集大量有关钢铁的成语与民间谚语.其中有说明钢的性能比铁好的有
恨铁不成钢
,知道“百炼成钢”是指铁在高温条件下反复敲打发生的反应是:C+O2═CO2
,从而了解钢与铁的机械性能不同是因为两者含碳量不等
.(9)钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究.
[提出假设]a. Ti的金属活动性比Mg强;
b.Ti的金属活动性介于Mg和Ag之间.
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速率越快,则该金属活动性越强.
[实验设计]同温下,取大小相同的这三种金属薄片,分别投入等体积、等浓度的足量稀盐酸中,观察现象.
请回答:三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是
除去氧化膜利于直接反应
.[实验现象]

[实验结论]原假设中
a
不正确,理由是镁反应速率比钛快
.[结论]用不同浓度的足量稀盐酸反应,是否也能得出同样结论?
否
,请说明理由反应速率与反应物浓度有关
(10)小刚与小红分别做相同质量的不同金属与同质量、同质量分数的稀H2SO4反应的实验,实验
结束后,分别交上的实验报告,并绘制出金属Zn、Fe分别与稀H2SO4反应放出H2的函数图象(如图所示).

两个图象中存在有错误的是
小红
的图象,判断错误的理由是图象中Fe与Zn标反了,Zn的反应速率较Fe快
,图象不同的原因是
小刚取的金属量较少,金属反应完,而小红取的酸量较少,酸完全反应完
.由该实验可以得到的结论:
①金属与酸反应的速率与
金属活动性
有关.②金属与酸反应中若生成盐中金属价态相同,则生成的氢气量与
相对原子质量
有关.(11)将铁粉加到一定量的硝酸银、硝酸铜、硝酸锌的混合溶液中,充分反应后过滤,在滤液中滴加盐酸,没有白色沉淀生成,则滤渣中一定有
Ag、Zn(NO3)2
,肯定滤液中有Fe(NO3)2
.(12)现一块铜合金,可能是黄铜(铜锌合金)、青铜(铜、锡合金)、白铜[铜、镍(Ni)合金]中的一
种,现欲测定其组成.
[查阅资料]Ⅰ.锌、锡、镍皆能与稀硫酸发生置换反应,生成+2价的金属离子;
Ⅱ.相对原子质量Zn-65,Sn一119,Ni一59.
[实验步骤及数据]取5g合金粉碎后放入烧杯中,将20g15%稀H2SO4分四次加入烧杯中充分反应后,测定剩余固体质量数据记录如下:

试求:①合金中铜的质量分数
64%
.②合金中另一金属为何种金属.另一种金属为锌
.阅读下列信息,回答有关问题:
材料1:三聚氰胺是一种重要的氮杂环有机化工原料.简称三胺,俗称蜜胺、蛋白精,其化学式为 C3H6N6.三聚氰胺为白色晶体,无味,密度1.57g/cm3,微溶于水.低毒,常温稳定,高温可分解,放出有毒的氰化物.三聚氰胺最主要的用途是作为生产三聚氰胺甲醛树脂(MF)的原料.三聚氰胺还可以作阻燃剂、减水剂、甲醛清洁剂等.
材料2:三鹿奶粉加入三聚氰胺后使奶粉的含氮量增大,以此冒充蛋白质.牛奶呈中性或微酸性,而三聚氰胺的水溶液呈碱性.目前较多采用尿素[CO(NH2)2]在高温环境下反应生成三聚氰胺,同时得到氨气(NH3)和二氧化碳.生成的三聚氰胺粗品.经热水溶解,过滤,冷却结晶后制成成品.
回答下列问题:
(1)三聚氰胺的物理性质有:
(2)三聚氰胺的化学性质有:
(3)三聚氰胺的相对分子质量为
(4)奶粉中蛋白质的含氮量约为16%;三聚氰胺被人称为“蛋白精”,价格便宜.牛奶和奶粉添加三聚氰胺,主要是因为它能冒充蛋白质.试解释三聚氰胺可以冒充蛋白质的原因:
(5)工业上一般采用尿素法生成三聚氰胺,根据上述信息写出该反应的化学方程式:
(6)为安全起见,一般采用三聚氰胺制造的食具都会标明“不可放进微波炉使用”.试解释相关原因:
(7)请你从分子原子的角度分析:三聚氰胺升华和三聚氰胺在高温下分解放出氰化物,有何本质区别?
查看习题详情和答案>>
材料1:三聚氰胺是一种重要的氮杂环有机化工原料.简称三胺,俗称蜜胺、蛋白精,其化学式为 C3H6N6.三聚氰胺为白色晶体,无味,密度1.57g/cm3,微溶于水.低毒,常温稳定,高温可分解,放出有毒的氰化物.三聚氰胺最主要的用途是作为生产三聚氰胺甲醛树脂(MF)的原料.三聚氰胺还可以作阻燃剂、减水剂、甲醛清洁剂等.
材料2:三鹿奶粉加入三聚氰胺后使奶粉的含氮量增大,以此冒充蛋白质.牛奶呈中性或微酸性,而三聚氰胺的水溶液呈碱性.目前较多采用尿素[CO(NH2)2]在高温环境下反应生成三聚氰胺,同时得到氨气(NH3)和二氧化碳.生成的三聚氰胺粗品.经热水溶解,过滤,冷却结晶后制成成品.
回答下列问题:
(1)三聚氰胺的物理性质有:
白色晶体,无味,密度1.57g/cm3,微溶于水
白色晶体,无味,密度1.57g/cm3,微溶于水
.(2)三聚氰胺的化学性质有:
低毒,常温稳定,高温可分解,放出有毒的氰化物.
低毒,常温稳定,高温可分解,放出有毒的氰化物.
.(3)三聚氰胺的相对分子质量为
126
126
;三聚氰胺中氮元素的质量分数为66.7%
66.7%
.(4)奶粉中蛋白质的含氮量约为16%;三聚氰胺被人称为“蛋白精”,价格便宜.牛奶和奶粉添加三聚氰胺,主要是因为它能冒充蛋白质.试解释三聚氰胺可以冒充蛋白质的原因:
三聚氰胺是一种白色结晶粉末,没有气味和味道,掺杂后不易被发现,价格便宜
三聚氰胺是一种白色结晶粉末,没有气味和味道,掺杂后不易被发现,价格便宜
;不法分子通常在奶粉中添加三聚氰胺,而不是在液态牛奶中添加,原因是三聚氰胺微溶于水,在液体牛奶中添加会造成牛奶中出现沉淀
三聚氰胺微溶于水,在液体牛奶中添加会造成牛奶中出现沉淀
.(5)工业上一般采用尿素法生成三聚氰胺,根据上述信息写出该反应的化学方程式:
6CO(NH2)2
C3H6N6+3CO2↑+6NH3↑
| ||
| △ |
6CO(NH2)2
C3H6N6+3CO2↑+6NH3↑
.
| ||
| △ |
(6)为安全起见,一般采用三聚氰胺制造的食具都会标明“不可放进微波炉使用”.试解释相关原因:
三聚氰胺在高温下可能会分解放出氰化物,氰化物通常具有毒性
三聚氰胺在高温下可能会分解放出氰化物,氰化物通常具有毒性
.(7)请你从分子原子的角度分析:三聚氰胺升华和三聚氰胺在高温下分解放出氰化物,有何本质区别?
三聚氰胺升华时,分子本身没有发生变化,只是分子间的间隔发生了改变;三聚氰胺在高温下分解,分子本身发生的变化,三聚氰胺分子分成原子,原子再组合成新分子
三聚氰胺升华时,分子本身没有发生变化,只是分子间的间隔发生了改变;三聚氰胺在高温下分解,分子本身发生的变化,三聚氰胺分子分成原子,原子再组合成新分子
.“家事国事天下事事事关心”.作为新时代的中学生,我们不仅要学习文化知识,而且要关注社会,关注生活.
(1)2013年4月20日8点02分四川省雅安市芦山县发生7.0级地震.地震发生后,全国人民抗震救灾,众志成城,彰显了中华民族巨大的凝聚力.
①救灾需要大量的消毒剂,我国研制出比漂白粉更高效的饮用水消毒剂“ClO2”,其反应的微观过程图如下:

(其中 表示氯原子,
表示氯原子, 表示钠原子,
表示钠原子, 表示氧原子)
表示氧原子)
试回答:ClO2叫做______,其中氯的化合价为______价.
根据反应的微观过程图写出反应的化学方程式为______.
②国家药监局公布的抗震救灾急需药械目录中包括:一次性防护服、活性炭防护口罩、骨科内外固定材料等.其中防护口罩主要是利用活性炭的______性.
③地震发生后,全国各地为灾区紧急提供包括方便面在内的各种救灾物品.据下表回答:
| 方便面营养成分表(每100g中含量) | |||||||||
| 糖类 (g) | 脂肪 (g) | 蛋白质 (g) | 水分 (g) | 钠 (mg) | 钾 (mg) | 磷 (mg) | 钙 (mg) | 维生素C (mg) | 其他 |
| 61.6 | 21.1 | 9.5 | 3.6 | 1144 | 134 | 80 | 25 | 0 | … |
(2)有机高分子材料、金属材料和无机非金属材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要.
①有机高分子材料“玉米塑料”因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少“______污染”.
②金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于______变化(选填“物理”或“化学”).
③无机非金属材料中,用于电子工业的高纯碳酸钙和高纯氧化钙生产流程如下:

实验室常采用______操作进行沉淀分离,生产高纯碳酸钙时,选择“220℃恒温干燥”,而不选择“高温”条件下完成此操作的原因是______(用化学方程式说明).
(3)创新利用CO2,倡导低碳生活,发展低碳经济已成为一种环保时尚.现在许多城市倡导“135”出行,即1公里以内步行,3公里以内骑自行车,5公里乘坐公共交通工具,提倡“低碳城市”、“绿色出行”.
①为减少CO2排放,人们积极寻找不含碳元素的燃料.经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景.请将NH3燃烧反应的化学方程式补充完整:4NH3+3O2
 6H2O+______.
6H2O+______.②法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O.试写出该反应的化学方程式______. 查看习题详情和答案>>