题目内容
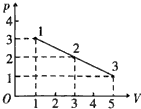 一定质量的理想气体,经历了如图所示的状态变化1→2→3过程,则三个状态的温度之比是
一定质量的理想气体,经历了如图所示的状态变化1→2→3过程,则三个状态的温度之比是分析:本题可根据理想气体状态方程
=C,分析T与pV的关系.
| PV |
| T |
解答:解:根据理想气体状态方程
=C,得:T∝pV.
则得:1、2、3三个状态的温度之比为:T1:T2:T3=p1V1:p2V2:p3V3=3×1:2×3:1×5=3:6:5.
故答案为:3:6:5
| PV |
| T |
则得:1、2、3三个状态的温度之比为:T1:T2:T3=p1V1:p2V2:p3V3=3×1:2×3:1×5=3:6:5.
故答案为:3:6:5
点评:解决本题的关键掌握理想气体状态方程
=C,知道T∝pV.
| PV |
| T |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法中不正确的是( )
| A、布朗运动是由液体分子从各个方向对悬浮粒子撞击作用的不平衡引起的 | B、对于一定质量的理想气体,若单位体积内分子个数不变,当分子热运动加剧时,压强一定变大 | C、当两个分子间的距离为r0(平衡位置)时,分子势能最小且一定为零 | D、单晶体和多晶体均存在固定的熔点 |
 一定质量的理想气体,从初始状态A经状态B、C、D再回到状态A,其体积V与温度T的关系如图所示.图中TA、VA和TD为已知量.
一定质量的理想气体,从初始状态A经状态B、C、D再回到状态A,其体积V与温度T的关系如图所示.图中TA、VA和TD为已知量. 【物理--选修3-3】
【物理--选修3-3】