0 99686 99694 99700 99704 99710 99712 99716 99722 99724 99730 99736 99740 99742 99746 99752 99754 99760 99764 99766 99770 99772 99776 99778 99780 99781 99782 99784 99785 99786 99788 99790 99794 99796 99800 99802 99806 99812 99814 99820 99824 99826 99830 99836 99842 99844 99850 99854 99856 99862 99866 99872 99880 203614
 2OH-+ H2↑+ Cl2↑
2OH-+ H2↑+ Cl2↑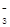
 + HCO
+ HCO + CO2↑
+ CO2↑

 2H+ + Cl-+ClO-
2H+ + Cl-+ClO-
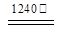 2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。
2Al2O3 + 2NH3↑+ N2↑+ 5SO3↑+ 3SO2↑+ 53H2O,将产生的气体通过下图所示的装置。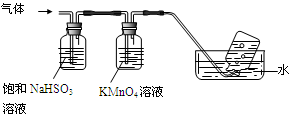

 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O SO2↑+Cl2↑+H2O
SO2↑+Cl2↑+H2O )既有氧化性又有还原性
)既有氧化性又有还原性 NH3↑+H2O
NH3↑+H2O