下列各组物质的无色溶液,不用其它试剂即可鉴别的是( )
①KOH Na2SO4 AlCl3 ②NaHCO3 NaNO3 H2SO4
③HCl NaAlO2 NaCl ④Ca(OH)2 Na2CO3 BaCl2
| A.①③ | B.②③ | C.①④ | D.①② |
物质制备过程中离不开物质的提纯。以下除杂方法不正确的是
| 选项 | 目的 | 实验方法 |
| A | 除去Na2CO3固体中的NaHCO3 | 置于坩埚中加热至恒重 |
| B | 除去NaCl中少量KNO3 | 将混合物制成热饱和溶液,冷却结晶,过滤 |
| C | 除去CO2中的HCl气体 | 通过NaHCO3(aq,饱和),然后干燥 |
| D | 除去C2H5Br中的Br2 | 加入足量Na2SO3(aq),充分振荡,分液 |
为了证明硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]晶体的成分中含有NH4+、Fe2+、SO42-和H2O,下列实验叙述中不正确的是
| A.取少量硫酸亚铁铵晶体放入试管中,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水 |
| B.取少量硫酸亚铁铵晶体放入试管,加浓NaOH溶液,加热,试管口湿润的蓝色石蕊试纸变红,则可证明晶体的成分中含有NH4+ |
| C.取适量硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
| D.取适量硫酸亚铁铵晶体溶于水,得浅绿色溶液,滴入2滴KSCN溶液,溶液不显血红色,再滴入几滴新制氯水,溶液变为血红色,则可证明晶体的成分中含有Fe2+ |
用酸性KMnO4溶液不能达到预期目的的是
| A.区别苯和甲苯 |
| B.检验硫酸铁溶液中是否有硫酸亚铁 |
| C.检验CH2=CHCHO中含碳碳双键 |
| D.区别SO2和CO2 |
甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成。已知:
①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;
②0.1 mol/L乙溶液中c(H+)>0.1 mol/L;
③向丙溶液中滴入AgNO3溶液,有不溶于稀HNO3的白色沉淀生成。
下列结论错误的是
| A.甲溶液含有Ba2+ | B.乙溶液含有SO42- |
| C.丙溶液含有Cl- | D.丁溶液含有Mg2+ |
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。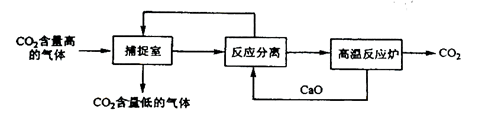
下列有关该方法的叙述中错误的是
| A.能耗大是该方法的一大缺点 |
| B.整个过程中,有两种物质可以循环利用 |
| C.捕捉到的CO2可用来制备甲醇等产品,可减少碳排放 |
| D.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤 |
下列除杂分离方法正确的是
| 选项 | 物质 | 杂质 | 所用试剂 | 分离方法 |
| A. | KCl | CaCl2 | Na2CO3溶液、盐酸 | 过滤 |
| B. | CH3CH2OH | CH3COOH | CaO | 蒸馏 |
| C. | NaCl | NH4Cl | NaOH | 蒸干 |
| D. | N2 | O2 | 铜网 | 加热 |
下列实验中,依据实验操作及现象,得出的结论正确的是
| | 操作 | 现 象 | 结 论 |
| A. | 测定等浓度的Na2CO3和Na2SO3 溶液的pH | 前者pH比后者的大 | 非金属性: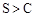 |
| B. | 无色溶液中滴加氯水和CCl4, 振荡、静置 | 下层溶液显紫色 | 原溶液中有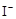 |
| C. | 向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有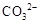 或 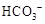 |
| D. | 向某无色溶液中滴加硝酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中一定含有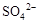 |
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示)。
下列有关说法不正确的是
| A.从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能量的过程 |
| B.过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2 |
| C.在过程③⑤中溴元素均被氧化 |
| D.过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
下图所示的实验操作,装置或操作存在错误不能达到相应目的的是
 |  |  |  |
| A.从NaCl溶液提取NaCl固体 | B.实验室中制取少量蒸馏水 | C.闻氯气的气味 | D.分离油和水混合物 |