题目内容
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。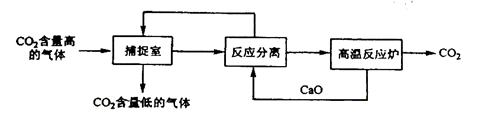
下列有关该方法的叙述中错误的是
| A.能耗大是该方法的一大缺点 |
| B.整个过程中,有两种物质可以循环利用 |
| C.捕捉到的CO2可用来制备甲醇等产品,可减少碳排放 |
| D.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤 |
D
解析试题分析:A、该方法过程中需高温分解石灰石制备氧化钙,故能耗大,正确;B、该过程中氢氧化钠、碳酸钙回收循环利用,正确;C、正确;D、该环节中生成的难溶物碳酸钙,直接过滤洗涤即可,错误。
考点:考查物质的转化有关问题。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是
(1)过滤 (2)加过量的NaOH溶液 (3)加适量HCl (4)加过量的Na2CO3溶液
(5)加过量的BaCl2溶液
| A.(2)(3)(4)(5)(1) | B.(4)(1)(2)(5)(3) |
| C.(2)(5)(4)(1)(3) | D.(5)(2)(4)(3)(1) |
只用一种试剂即可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、(NH4)2SO4五种溶液,这种试剂是
| A.BaCl2 | B.H2SO4 | C.NaOH | D.AgNO3 |
有一瓶乙二醇和丙三醇的混合物,它们的性质如下表。则将乙二醇和丙三醇互相分离的最佳方法是
| 物质 | 分子式 | 熔点/℃ | 沸点/℃ | 密度/g·cm-1 | 溶解性 |
| 乙二醇 | C2H4O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
A.分液 B.蒸馏 C.冷却至0℃后过滤 D.加水萃取
下列实验操作能达到目的的是
| A.除去苯中混有的少量苯酚:加入适量NaOH溶液,振荡、静置后分液 |
| B.除去乙酸乙酯中混有的少量乙酸:加入NaOH溶液并加热,振荡、静置后分液 |
| C.检验卤代烃中的卤原子:取少量液体与NaOH溶液共热后滴加AgNO3溶液 |
| D.检验FeCl3溶液中是否含有Fe2+:取少量溶液先滴加氯水,再滴加KSCN溶液 |
下列各组物质的无色溶液,不用其它试剂即可鉴别的是( )
①KOH Na2SO4 AlCl3 ②NaHCO3 NaNO3 H2SO4
③HCl NaAlO2 NaCl ④Ca(OH)2 Na2CO3 BaCl2
| A.①③ | B.②③ | C.①④ | D.①② |
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示)
下列有关说法正确的是
A.第①步中除去粗盐中的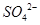 、 、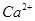 、 、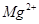 、 、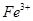 等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaC12溶液→过滤后加盐酸 等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaC12溶液→过滤后加盐酸 |
B.第②步中结晶出的MgC12 6H2O可在空气中受热分解制无水MgC12 6H2O可在空气中受热分解制无水MgC12 |
| C.从第③步到第⑤步的目的是浓缩 |
| D.在第③④⑤步中溴元素均被氧化 |
利用实验器材(规格和数量不限),能完成相应实验的一项是
| | 实验器材(省略夹持装置) | 相应实验 |
| A | 烧杯、玻璃棒、蒸发皿 | 硫酸铜溶液的浓缩结晶 |
| B | 烧杯、玻璃棒、胶头滴管、滤纸 | 用盐酸除去硫酸钡中的少量碳酸钡 |
| C | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用固体氯化钠配制0.5mol/L的溶液 |
| D | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中的少量NaI |
在有B离子存在的情况下,欲用试剂C来检验溶液中是否含有A离子,下表所加试剂C能够对A离子进行成功检验的是(说明:在实验过程中不允许加热、过滤、萃取等操作)
| 选项 | 试剂C | A离子 | B离子 |
| A | HNO3、BaCl2 | SO42- | SO32- |
| B | AgNO3 | Cl- | I- |
| C | KSCN | Fe2+ | Fe3+ |
| D | NH3?H2O | Al3+ | Ag+ |