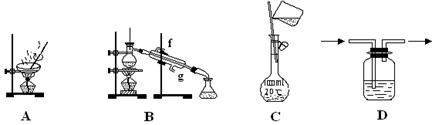
下列实验操作或原理不正确的是
| A.读取滴定管内液体体积时,俯视读数导致读数偏小 |
| B.分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 |
| C.纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 |
| D.进行焰色反应时,必须用稀硫酸洗涤并灼烧铂丝,然后再进行实验 |
如右图所示装置进行实验(图中铁架台等仪器均已略去)。在Ⅰ中加入试剂后,塞紧橡皮塞,立即打开止水夹,Ⅱ中有气泡冒出;一段时间后关闭止水夹,Ⅱ中液面上升,溶液由无色变为浑浊。不符合以上实验现象的Ⅰ和Ⅱ中应加入的试剂是 ( )
| | A | B | C | D |
| Ⅰ | CaCO3、稀HCl | NaHCO3、稀H2SO4 | Fe、稀H2SO4 | Al、稀NaOH |
| Ⅱ | AgNO3 | MgCl2 | NaOH | AlCl3 |
下列实验装置设计正确、且能达到目的的是( )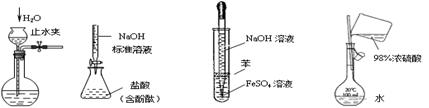
Ⅰ Ⅱ Ⅲ Ⅳ
| A.实验I: 检查装置的气密性 |
| B.实验II:测定未知盐酸的浓度 |
| C.实验III:制取并观察Fe(OH)2沉淀 |
| D.实验IV:配置一定的物质的量浓度的稀硫酸溶液 |
下列实验操作与对应的反应现象或原理正确的一组是( )
| 选项 | 实验操作 | 现象或原理 |
| A | 取少量KI溶液,先滴加氯水,再加入少量苯,振荡、静置 | 溶液分层,下层呈紫红色 |
| B | 将稀盐酸或氢氧化钠溶液慢慢滴入氢氧化铝胶体中 | 均先沉淀后溶解 |
| C | 将浓硝酸加入盛有铂、金的烧杯中,不反应,加入一定量浓盐酸后,铂、金溶解 | 浓盐酸氧化性强于浓硝酸 |
| D | 将40.0 g NaOH固体溶于1.0 L蒸馏水中配成溶液 | 溶液物质的量浓度为1.0mol﹒L-1 |
研究物质的性质有四个基本主干程序,是一个系统化的研究过程。研究金属镍的性质的基本程序的第三步是
| A.预测物质的性质 | B.进行实验和观察 |
| C.观察物质的外观特征 | D.做出有关的解释和结论 |
下列针对甲、乙、丙、丁四种实验及装置的说法,不合理的是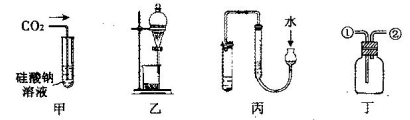
| A.甲可用来证明碳的非金属性比硅强 |
| B.乙装置可用于碘水中碘的萃取及分液 |
| C.用丙图示的方法检查此装置的气密性 |
| D.丁装置:从①进气可收集NO;从②进气可收集NH3 |
既能用浓硫酸又能用碱石灰干燥的气体是
| A.Cl2 | B.SO2 | C.CO | D.NH3 |
下列说法正确的是
| A.用广泛pH试纸测得饱和氯水的pH约为2.2 |
| B.配制一定物质的量浓度的溶液,定容时仰视刻度,溶液浓度偏小 |
| C.用待测液润洗锥形瓶后才能进行滴定操作 |
| D.中和反应热测定实验中,要将盐酸逐滴加入烧碱溶液 |
下列叙述合理的是
| A.用溴的四氯化碳溶液除去甲烷中混有的少量乙烯气体 |
| B.向淀粉溶液中加入稀硫酸,加热几分钟,冷却后再加入少量新制Cu(OH)2浊液,加热, 没有红色沉淀生成,说明淀粉还没有发生水解 |
| C.用硝酸酸化的AgNO3溶液检验否含有氯元素 |
| D.红热的铜丝可以和乙醇发生置换反应产生氢气 |