如下各图烧杯中盛有海水,铁在其中被腐蚀由快到慢的顺序为 ( )
| A.②①③④ | B.④③②① |
| C.④②①③ | D.③②④① |
如图所示,将铁棒和石墨棒插入1L 1mol﹒L-1食盐水中。下列说法正确的是( )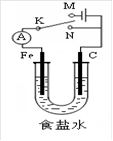
| A.若电键K与N连接,铁被保护不会腐蚀 |
| B.若电键K与N连接,正极反应式是4OH- -4e-=2H2O+O2↑ |
| C.若电键K与M连接,将石墨棒换成铜棒可实现铁棒上镀铜 |
| D.若电键K与M连接,当两极共产生28 L(标准状况)气体时,生成1 mol NaOH |
如图为用惰性电极电解CuCl2溶液,并验证其产物的实验装置,则下列说法不正确的是 ( )
| A.电源a极为负极 |
| B.KI—淀粉溶液会变蓝 |
| C.可以将惰性电极Ⅰ换为铜棒 |
| D.惰性电极Ⅰ上发生的电极反应为:Cu-2e-=Cu2+ |
下图为Mg—NaClO燃料电池结构示意图。下列说法正确的是( )
| A.镁作Y电极 |
| B.电池工作时Na+向负极移动 |
| C.废液的pH大于NaClO溶液的pH |
| D.X电极上发生的反应为:ClO-+2H2O-4e-= ClO3-+4H+ |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B.1 mol OH-在电解过程中完全放电时电路中通过了NA个电子 |
| C.铜的电解精炼时,阳极上每转移2mol电子时就溶解铜原子NA个 |
| D.1mol/L的Na2CO3溶液中CO32-粒子数目小于NA |
图中两电极上发生的电极反应如下:a极:Cu2++2e-=Cu,b极:Fe-2e-=Fe2+,则以下说法不正确的是( )
| A.该装置可能是电解池 |
| B.a极上一定发生还原反应 |
| C.a、b可能是同种电极材料 |
| D.该过程中能量的转换一定是化学能转化为电能 |
实验发现,在FeCl3酸性溶液中加入少量锌粉后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如图所示的原电池装置。下列有关说法中正确的是( )
| A.该原电池的正极反应是:Zn-2e— =Zn2+ |
| B.Pt电极表面生成大量气泡 |
| C.左烧杯中溶液的红色逐渐褪去 |
| D.生成的Fe2+通过盐桥可以和锌直接反应生成Fe |
用惰性电极电解下列足量溶液,一段时间后,再加入一定量的另一种物质(括号内物质),溶液与原来溶液完全一样的是 ( )
| A.NaCl(盐酸) | B.NaOH(NaOH) | C.AgNO3(Ag2O) | D.CuSO4[Cu(OH)2] |
下图甲池和乙池中的四个电极都是铂电极,乙池溶液分层,上层溶液为盐溶液,呈中性。请根据图示判断下列有关说法正确的是:
| A.甲池的电解池,乙池是原电池 |
| B.通入乙醇的铂电极反应式为C2H5OH+16OH-+12e-=2CO32-+11H2O |
| C.反应一段时间后,两池溶液的pH均未变化 |
| D.假如乙池中加入NaI溶液,则在乙池反应过程中,可以观察到C电极周围的溶液呈现棕黄色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色 |
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是
| A.电池放电时Na+从a极区移向b极区 |
| B.每消耗3 mol H2O2,转移的电子为3 mol |
| C.电极a采用MnO2,MnO2既作电极材料又有催化作用 |
| D.该电池的负极反应为:BH4-+2H2O-8e-=BO2-+8H+ |