人工肾脏可用间接电化学方法除去代谢产物中的尿素[(CO(NH2)2) ],即通过阳极反应生成具有强氧化作用的中间产物来氧化代谢产物,原理如右图所示,下列说法正确的是
| A.B为 电 源 的正 极 |
| B.电解过程中,阳极室附近的PH保持不变 |
| C.电解过程中,电子由电源B端流出经溶液流回到电源A端 |
| D.右边发生的电极反应式为:2H2O +2e-= H2↑+ 2OH- |
如图为一原电池的结构示意图,下列说法中,不正确的是
| A.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu |
| B.原电池工作时,Zn电极流出电子,发生氧化反应 |
| C.原电池工作时,铜电极上发生氧化反应,CuSO4溶液蓝色变深 |
| D.盐桥中阳离子流向CuSO4溶液中 |
氢镍电池是一种碱性可充电电池,污染小,比能量较大。氢镍电池的总反应式是:
H2+2NiO(OH) 2Ni(OH)2。据此反应式判断,下列叙述中正确的是
2Ni(OH)2。据此反应式判断,下列叙述中正确的是
| A.电池放电时,H2是正极 |
| B.电池充电时,镍元素被还原 |
| C.充电时,电池负极的电极反应式为2H2O+2e—=H2+2OH— |
| D.电池放电时,H2是负极,负极周围溶液的pH不断增大 |
研究人员最近发现了一种“水”电池,这种电池能利用淡水和海水之间含盐量的差别进行发电,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是
| A.Ag发生还原反应 |
| B.正极反应式:5MnO2+2e- =Mn5O102- |
| C.每生成1mol AgCl转移2mol电子 |
| D.Cl—不断 向“水”电池的正极移动 |
对于下图的锌锰电池,下列说法正确的是
| A.MnO2是氧化剂,被氧化 |
| B.碳棒为负极、锌筒为正极 |
| C.放电过程中NH4+向锌极移动 |
| D.负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2(s)+Pb(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(I),根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb+SO42--2e-=PbSO4↓ |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
某原电池总反应为:Cu+2Fe3+=Cu2++2Fe2+下列能实现该反应的原电池是
| | A | B | C | D |
| 电极材料 | Cu、Zn | Cu、Ag | Cu、C | Fe、Zn |
| 电解液 | FeCl3 | Fe2(SO4)3 | Fe(NO3)2 | CuSO4 |
有关如右图所示原电池(盐桥中装有含琼胶的KCl饱和溶液)的叙述,不正确的是
| A.铜片上有红色物质附着 |
| B.取出盐桥后,电流计依然发生偏转 |
| C.反应中,盐桥中的K+会移向CuSO4溶液 |
| D.锌片上发生氧化反应 |
体积为1 L的某溶液中含有的离子如表所示:
| 离子 | Cu2+ | Al3+ | NO3— | Cl- |
| 物质的量浓度 mol/L | 1 | 1 | a | 1 |
用Pt电极电解该溶液,当电路中有3 mol电子通过时(忽略电解时溶液体积的变化及电解产物可能存在的溶解现象),下列说法正确的是 ( )。
A.电解后溶液的pH=0
B.a=3
C.阳极生成1.5 mol Cl2
D.阴极析出的金属是铜与铝
利用如图装置可以模拟铁的电化学防护。下列叙述正确的是 ( )。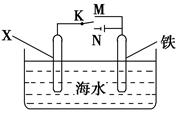
| A.铁被腐蚀过程实质是金属铁发生了还原反应 |
| B.若X为锌片,开关K置于M处,可减缓铁的腐蚀 |
| C.若X为碳棒,开关K置于M处,可减缓铁的腐蚀 |
| D.当K置于N处时,可减缓铁的腐蚀 |