如图所示,杠杆AB两端分别挂有体积相同、质量相同的空心铜球和空心铁球,调节杠杆使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中不考虑铁丝反应及两边浮力的变化)( )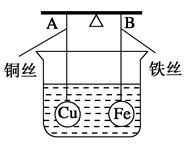
| A.杠杆为导体和绝缘体时,均为A端高B端低 |
| B.杠杆为导体和绝缘体时,均为A端低B端高 |
| C.当杠杆为绝缘体时,A端低B端高;为导体时,A端高B端低 |
| D.当杠杆为绝缘体时,A端高B端低;为导体时,A端低B端高 |
某原电池总反应离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
| A.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液 |
| B.正极为C,负极为Fe,电解质溶液为Fe(NO3)3溶液 |
| C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液 |
| D.正极为Ag,负极为Fe,电解质溶液为CuSO4溶液 |
如图所示装置中,可观察到电流计指针偏转,M棒变粗,N棒变细。下表所列M、N、P物质中,可以组合成该装置的是( )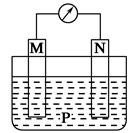
| 选项号 | M | N | P |
| A | 锌 | 铜 | 稀硫酸 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。下列说法中正确的是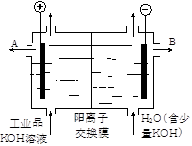
| A.该电解槽的阳极反应式是4OH--2e-→2H2O+ O2↑ |
| B.通电开始后,阴极附近溶液pH会减小 |
| C.除去杂质后氢氧化钾溶液从液体出口A导出 |
| D.用氯化钾制备氢氧化钾也可采用这种离子交换膜电解法 |
下图为两个原电池装置图,由此判断下列说法错误的是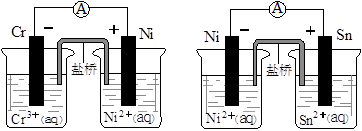
| A.当两电池转移相同电子时,生成和消耗Ni的物质的量相同 |
| B.两装置工作时,盐桥中的阴离子向负极移动,阳离子向正极移动 |
| C.由此可判断能够发生2Cr3++3Ni=3Ni2++2Cr和Ni2++Sn=Sn2++Ni的反应 |
| D.由此可判断Cr、Ni、Sn三种金属的还原性强弱顺序为:Cr>Ni>Sn |
如下图所示的两个实验装置,溶液的体积均为200mL。开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液的体积变化,下列叙述中正确的是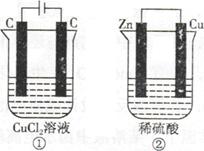
| A.产生气体的体积:①>② |
| B.溶液的pH变化:①减小,②增大 |
| C.电极上生成物质的质量:①=② |
| D.电极反应式:①中阳极2Cl—-2e—=Cl2↑,②中负极2H++2e—=H2↑ |
如图所示,用铁棒和石墨棒作电极电解1L 1mol/L食盐水,下列有关说法 正确的是 ( )
| A.电键K与N连接,铁棒被保护而免受腐蚀 |
| B.电键K与N连接,正极反应式为:4OH--4e-=2H2O +O2 ↑ |
| C.电键K与M连接,将石墨棒换成铜棒,就可实现在铁棒上镀铜 |
| D.电键K与M连接,当两极共产生标准状况下气体33.6L时,理论上生成lmol NaOH |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
下列叙述不正确的是( )
| A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B.放电时正极反应为:FeO42-+4H2O+3e-=Fe(OH)3+5OH- |
| C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是( )
| A.正极反应式为O2+2H2O+4e-=4OH- |
| B.电池工作时,电流由铝电极沿导线流向铂电极 |
| C.以网状的铂为正极,可增大与氧气的接触面积 |
| D.该电池通常只需要换铝板就可以继续使用 |