题目内容
如图所示,用铁棒和石墨棒作电极电解1L 1mol/L食盐水,下列有关说法 正确的是 ( )
| A.电键K与N连接,铁棒被保护而免受腐蚀 |
| B.电键K与N连接,正极反应式为:4OH--4e-=2H2O +O2 ↑ |
| C.电键K与M连接,将石墨棒换成铜棒,就可实现在铁棒上镀铜 |
| D.电键K与M连接,当两极共产生标准状况下气体33.6L时,理论上生成lmol NaOH |
D
解析试题分析:A.电键K与N连接,构成的是原电池,Fe的活动性比C强,作负极,被氧化而受腐蚀。错误。B.电键K与N连接,构成的原电池中由于NaCl溶液是中性介质,发生的是吸氧腐蚀。正极反应式为: O2 +4e-+2H2O =4OH-。错误。C.电键K与M连接,形成的是电解池。将石墨棒换成铜棒,铜棒作阳极,被氧化为Cu2+进入溶液,在阴极Fe上,2H++2e-=H2↑..错误。D.电键K与M连接,形成的是电解池,电解食盐水。n(气体)=1.5mol.反应的方程式为:2NaCl+2H2O 2NaOH+ H2↑+Cl2↑。n(NaCl)=1mol.所以当阳极产生n(Cl2)=0.5mol,阴极产生气体n(H2)=0.5mol时,NaCl消耗完全,这时的反应改为电解NaOH溶液,实质是电解水。2H2O
2NaOH+ H2↑+Cl2↑。n(NaCl)=1mol.所以当阳极产生n(Cl2)=0.5mol,阴极产生气体n(H2)=0.5mol时,NaCl消耗完全,这时的反应改为电解NaOH溶液,实质是电解水。2H2O 2H2↑+O2↑。NaOH的物质的量不变。根据元素守恒可得理论上生成lmol NaOH。正确。
2H2↑+O2↑。NaOH的物质的量不变。根据元素守恒可得理论上生成lmol NaOH。正确。
考点:考查原电池、电解池的反应原理的知识。

食品保鲜所用的“双吸剂”,是由还原铁粉、生石灰、氯化钠、炭粉等按一定比例组成的混合物,可吸收氧气和水。下列分析不正确的是
| A.“双吸剂”中的生石灰有吸水作用 |
| B.“双吸剂”吸收氧气时,发生了原电池反应 |
| C.吸收氧气的过程中,铁作原电池的负极 |
| D.炭粉上发生的反应为:O2+4e-+4H+=2H2O |
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是
| A.杠杆为导体或绝缘体时,均为A端高B端低 |
| B.杠杆为导体或绝缘体时,均为A端低B端高 |
| C.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低 |
| D.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高 |
下列叙述中正确的是( )。
| A.原电池的负极发生得电子的还原反应 |
| B.原电池中较活泼的金属作正极 |
| C.原电池中的电极一定要由两种不同的金属组成 |
| D.原电池中发生氧化反应的电极是负极 |
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-。下列对该燃料电池的说法中,正确的是( )
| A.在熔融的电解质中,O2-由负极移向正极 |
| B.电池的总反应是:2C4H10+13O2=8CO2+10H2O |
| C.通入空气的一极是正极,电极反应为O2+4e-=2O2- |
| D.通入丁烷的一极是正极,电极反应为C4H10+26e-+13O2-=4CO2+5H2O |
电化学在日常生活中用途广泛,图甲是镁—次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是( )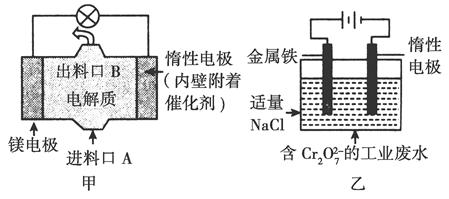
| A.图乙中Cr2O72-向惰性电极移动,与该极近的OH-结合转化成Cr(OH)3除去 |
| B.图乙的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生 |
| C.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓ |
| D.若图甲中3.6 g镁溶液产生的电量用以图乙废水处理,理论可产生10.7 g氢氧化铁沉淀 |
某课外活动小组用如图所示装置进行实验(电解液足量)。下列说法中错误的是( )
| A.图1中,若开始实验时开关K与a连接,则B极的电极反应式为Fe-3e-=Fe3+ |
| B.图1中,若开始实验时开关K与b连接,则一段时间后向电解液中通入适量HCl气体可恢复到电解前的浓度 |
| C.图2中,若开始实验时开关K与a连接,则电解液的溶质质量分数变小 |
| D.图2中,若开始实验时开关K与b连接,则A极减少的质量等于B极增加的质量 |
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
| A.甲醇 | B.天然气 | C.液化石油气 | D.氢气 |