以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是 ( )
| A.未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程 |
| B.因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |
| C.电镀时保持电流恒定,升高温度不改变电解反应速率 |
| D.镀锌层破损后即对铁制品失去保护作用 |
用石墨作电极电解200 mL CuSO4溶液,电解过程中电子转移的物质的量n(e-)与产生气体的体积V(g)(标准状况)的关系如图所示,下列说法正确的是 ( )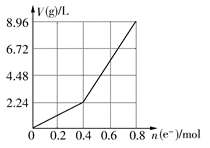
| A.电解前CuSO4溶液的物质的量浓度为2 mol/L |
| B.电解后所得溶液中c(H+)=2 mol/L |
| C.当n(e-)=0.6 mol时,V(H2):V(O2)=2:3 |
| D.向电解后的溶液中加入16 g CuO,则溶液可恢复为电解前的浓度 |
铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法中,不正确的是( )
| A.此过程中铜并不被腐蚀 |
| B.此过程中电子从Fe移向Cu |
| C.正极反应式为:2H++2e-=H2↑ |
| D.此过程中还涉及反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3 |
利用下图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是 ( )
| A.a管发生吸氧腐蚀,b管发生析氢腐蚀 |
| B.一段时间后,a管液面高于b管液面 |
| C.a处溶液的pH增大,b处溶液的pH减小 |
| D.a、b两处具有相同的电极反应式:Fe-2e-=Fe2+ |
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是 ( )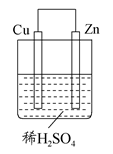

| A.①②③ | B.②④ | C.④⑤⑥ | D.③④⑤ |
某新型电池,以NaBH4(B的化合价为+3)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示。下列说法正确的是 ( )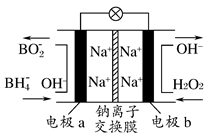
| A.电池工作时Na+从b极区移向a极区 |
| B.每消耗3 mol H2O2,转移3 mol e- |
| C.b极上的电极反应式为:H2O2+2e-+2H+=2H2O |
| D.a极上的电极反应式为:BH4—+8OH--8e-=BO2—+6H2O |
用吸附了氢气的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是 ( )
| A.放电时,负极的电极反应式为H2-2e-+2OH-=2H2O |
| B.充电时,阳极的电极反应式为Ni(OH)2+OH--e-=NiO(OH)+H2O |
| C.放电时,OH-移向镍电极 |
| D.充电时,将电池的碳电极与外电源的正极相连 |
原电池与电解池在生活和生产中有着广泛应用。下列有关判断中错误的是
装置① 装置② 装置③
| A.装置①研究的是电解CuCl2溶液,b电极上有红色固体析出 |
| B.装置②研究的是金属的吸氧腐蚀,Fe上的反应为Fe-2e- = Fe2+ |
| C.装置③研究的是电解饱和食盐水, B电极发生的反应:2Cl--2e- = Cl2↑ |
| D.三个装置中涉及的主要反应都是氧化还原反应 |
2013年12月31日夜,上海外滩运用LED产品进行了精彩纷呈的跨年灯光秀。下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是 
| A.a处通入氧气 |
| B.b处为电池正极,发生了还原反应 |
| C.该装置中只涉及两种形式的能量转化 |
| D.P-型半导体连接的是电池负极 |
