题目内容
利用下图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是 ( )
| A.a管发生吸氧腐蚀,b管发生析氢腐蚀 |
| B.一段时间后,a管液面高于b管液面 |
| C.a处溶液的pH增大,b处溶液的pH减小 |
| D.a、b两处具有相同的电极反应式:Fe-2e-=Fe2+ |
C
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
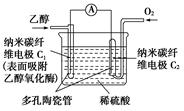
2013年12月31日夜,上海外滩运用LED产品进行了精彩纷呈的跨年灯光秀。下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是 
| A.a处通入氧气 |
| B.b处为电池正极,发生了还原反应 |
| C.该装置中只涉及两种形式的能量转化 |
| D.P-型半导体连接的是电池负极 |
早在1807年化学家戴维用电解熔融氢氧化钠制得钠:4NaOH(熔融)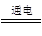 4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH
4Na+O2↑+2H2O;后来吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为3Fe+4NaOH 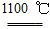 Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )
Fe3O4+2H2↑+4Na↑。下列有关说法正确的是 ( )
| A.电解熔融氢氧化钠制钠,阳极发生的电极反应为2OH--2e-=H2↑+O2↑ |
| B.若用戴维法与吕萨克法制得等量的钠,则两反应中转移的电子总数也相同 |
| C.吕萨克法制钠的原理是利用铁的还原性比钠强 |
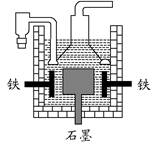
| D.目前工业上常用电解熔融氯化钠法制钠(如下图),电解槽中石墨为阳极,铁为阴极 |
如图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑点向d端扩散。下列判断正确的是( )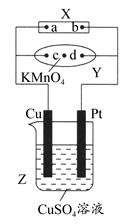
| A.滤纸上c点附近会变红色 |
| B.Cu电极质量减小,Pt电极质量增大 |
| C.Z中溶液的pH先减小,后增大 |
| D.溶液中的SO42—向Cu电极定向移动 |
下列有关电化学知识的描述正确的是 ( )
| A.CaO+H2O=Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B.某原电池反应为Cu+2AgNO3=Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液 |
| C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 |
钢铁生锈过程发生如下反应:①2Fe+O2+2H2O=2Fe(OH)2;②4Fe(OH)2+O2+2H2O=4Fe(OH)3;③2Fe(OH)3=Fe2O3+3H2O。下列说法正确的是( )。
| A.钢铁在碱性条件下腐蚀生成铁锈,而在酸性条件下不生成铁锈 |
| B.反应①中的氧化剂是氧气和水 |
| C.上述反应表示钢铁发生的是吸氧腐蚀 |
| D.钢铁在潮湿的空气中不能发生电化学腐蚀 |
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是( )。
| A.正极反应式为O2+2H2O+4e-=4OH- |
| B.电池工作时,电流由铝电极沿导线流向铂电极 |
| C.以网状的铂为正极,可增大与氧气的接触面积 |
| D.该电池通常只需更换铝板就可继续使用 |
 B;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为C2++2e-=C,B-2e-=B2+,则A、B、C、D金属性由强到弱的顺序为( )。
B;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为C2++2e-=C,B-2e-=B2+,则A、B、C、D金属性由强到弱的顺序为( )。