燃料电池是燃料(如CO、H2、CH4)等跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH)溶液,下列关于甲烷燃料电池的说法中不正确的是( )
| A.通入氧气的一极发生还原反应,通入甲烷的一极发生氧化反应 |
| B.负极的电极反应式为CH4+10OH--8e-=CO32—+7H2O |
| C.随着反应的进行,电解质溶液的pH保持不变 |
| D.甲烷燃料电池的能量利用率比甲烷燃烧的大 |
将金属a放入b(NO3)2溶液中发生如下反应:a+b2+=a2++b,则下列说法正确的是( )
| A.常温下,a或b可以与水发生反应 |
| B.a与b用导线连接插入稀H2SO4中,则形成原电池且b极上有H2放出 |
| C.a与b用导线连接插入b(NO3)2中一定构成原电池 |
| D.用惰性电极电解a(NO3)2与b(NO3)2的混合液,在阳极先析出b |
[双选题]下列说法正确的是( )
| A.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀 |
| B.原电池反应是导致金属腐蚀的主要原因,故不能用原电池原理来减缓金属的腐 蚀 |
| C.钢铁电化学腐蚀的两种类型主要区别在于水膜的酸性不同,引起的正极反应不同 |
| D.无论哪种类型的腐蚀,其实质都是金属被氧化 |
把等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,经充分搅拌后,将
所得溶液用石墨电极进行电解,阳极生成的物质是( )
| A.H2 | B.Ag | C.Cl2 | D.O2 |
关于如图所示装置的叙述,正确的是( )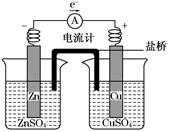
| A.铜是阳极,铜片上有气泡产生 |
| B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 |
| D.铜离子在铜片表面被还原 |
我国某大城市今年夏季多次降下酸雨。据环保部门测定,该城市整个夏季酸雨的pH平均为3.2。在这种环境中的铁制品极易被腐蚀。对此条件下铁的腐蚀的叙述不正确的是( )
| A.此腐蚀过程有化学腐蚀也有电化学腐蚀 |
| B.发生电化学腐蚀时的正极反应为 2H2O+O2+4e-=4OH- |
| C.在化学腐蚀过程中有氢气产生 |
| D.发生电化学腐蚀时的负极反应为Fe-2e-=Fe2+ |
下列是某校实验小组设计的一套原电池装置,下列有关描述不正确的是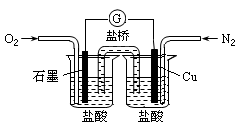
| A.此装置能将化学能转变为电能 |
| B.石墨电极的反应式:O2+2H2O+4e—=4OH— |
| C.电子由Cu电极经导线流向石墨电极 |
| D.电池总的反应是:2Cu+O2+4HCl=2CuCl2+2H2O |
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是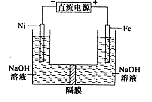
| A.铁是阳极,电极反应为Fe-6e一+4H2O=FeO42-+ 8H+ |
| B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 |
| C.若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计) |
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
| A.未通电前上述镀锌装置可构成原电池,电镀过程是该原电池的充电过程 |
| B.因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |
| C.电镀时保持电流恒定,升高温度不改变电解反应速率 |
| D.镀锌层破损后即对铁制品失去保护作用 |
某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
| A.正极反应式为:O2+2H2O+4e-=4OH- |
| B.工作一段时间后,电解液中KOH的物质的量不变 |
| C.该燃料电池的总反应方程式为:2H2+O2=2H2O |
| D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移 |