如图,有关零排放车载燃料电池叙述正确的是( )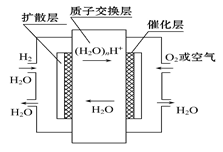
| A.正极通入H2,发生还原反应 |
| B.负极通入H2,发生还原反应 |
| C.导电离子为质子,且在电池内部由正极定向移向负极 |
| D.总反应式为2H2+O2 = 2H2O |
银锌纽扣电池的总反应式为Zn+Ag2O+H2O = Zn(OH)2+2Ag,下列说法不正确的是( )
| A.锌做负极 | B.放电时,正极产物是银 |
| C.电解质溶液不可能呈酸性 | D.充电时发生了原电池反应 |
生物燃料电池是以有机物为燃料,直接或简介利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿色电池。其工作原理如图所示。下列有关说法正确的是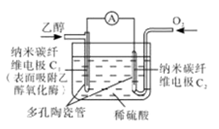
| A.O2在C2电极上得电子,被氧化 |
| B.电子由C2极经外电路流向C1极 |
| C.每转移6mole-,理论上生成22.4LCO2 |
| D.C1极的电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+ |
下列说法不正确的是:
| A.通过煤的干馏可获得苯、甲苯等芳香烃 |
| B.在海轮外壳装上锌块,可减缓船体的腐蚀速率 |
| C.电渗析法、离子交换法中,只有后者可以应用于海水的淡化 |
| D.我国城市推广使用清洁燃料是压缩天然气类和液化石油气类 |
硼化钒-空气电池是目前储电能力最高的电池,电池示意图如下图所示,该电池工作时的反应为:4 VB2+11O2===4B2O3+2V2O5,下列说法正确的是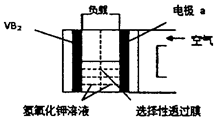
| A.电极a是电源负极 |
| B.溶液中的OH-向a极移动 |
| C.电子由VB2极经KOH溶液流向电极a |
| D.VB2极发生的电极反应为: |
下图是研究铁钉腐蚀的装置图。下列说法不正确的是
| A.ab在两处的腐蚀速率.a<b |
| B.a、b两处铁钉中的碳均为正极 |
| C.a、b两处铁钉中的铁均失电子被氧化 |
| D.a、b两处的正极反应式均为O2+4e-+ 4 H+=2H2O |
如图,石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质。图示装置工作时,生成的金属钙能还原二氧化钛制备金属钛。下列说法不正确的是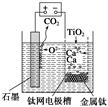
| A.阳极反应式为C + 2O2- - 4e-=CO2↑ |
| B.由TiO2制得1mol 金属Ti ,理论上外电路转移4 mol电子 |
| C.制备金属钛前后,装置中CaO的量不变 |
| D.TiO2在阴极放电 |
下列叙述不正确的是
| A.金属腐蚀的本质是金属原子失去电子而被氧化 |
| B.将地下钢管与直流电源的正极相连,用来保护钢管 |
| C.电解饱和食盐水制氢氧化钠,可以用铁做阴极 |
| D.氢氧燃料电池中,氢气在负极发生氧化反应 |
 Li2CoO2,下列说法不正确的是
Li2CoO2,下列说法不正确的是