已知温度T时,水的离子积常数为KW,该温度下,将浓度为a mol·L-1的一元酸HA溶液与b mol·L-1的一元碱BOH溶液等体积混合,可判定该溶液呈中性的依据是
| A.a=b |
| B.混合溶液的pH=7 |
C.混合溶液中,c(H+)=  mol·L-1 mol·L-1 |
| D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-) |
下列电解质溶液的有关叙述正确的是
| A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |
| B.在含有BaSO4沉淀的溶液中加入K2SO4固体,c(Ba2+)增大 |
| C.含l mol KOH的溶液与l mol CO2完全反应后,溶液中c(K+)>c(HCO3-) |
| D.在(NH4)2SO4溶液中加入适量H2SO4,可使c(NH4+)=2c(SO42-) |
0.1 mol·L-1NaOH溶液和0.1 mol·L-1NH4C1溶液等体积混合,离子浓度大小正确的是
| A.c(Na+)>c(C1-)>c(OH-)>c(H+) |
| B.c(Na+)=c(C1-)>c(OH-)>c(H+) |
| C.c(Na+)=c(C1-)>c(H+)>c(OH-) |
| D.c(C1-)>c(Na+)>c(OH-)>c(H+) |
相同体积的pH=3的强酸溶液和弱酸溶液分别跟足量的镁完全反应说法正确的,下列是
| A.弱酸溶液产生较多的氢气 |
| B.强酸溶液产生较多的氢气 |
| C.两者产生等量的氢气 |
| D.无法比较两者产生氢气的量 |
常温下0.1 mol·L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是
| A.将溶液稀释到原来体积的10倍 | B.加入适量的醋酸钠固体 |
| C.提高溶液的温度 | D.加入等体积0.2 mol·L-1盐酸 |
水中加入下列溶液对水的电离平衡不产生影响的是
| A.NaHSO4溶液 | B.KF溶液 | C.KAl(SO4)2溶液 | D.NaI溶液 |
25oC时,amol·L-1一元酸HA溶液与b mol·L-1 NaOH溶液等体积混合后,pH为7,则下列关系一定正确的是
| A.a=b | B.a>b | C.c(A-)=c(Na+) | D.c(A-)<c(Na+) |
下列化学方程式中,属于水解反应的是
A.HCOOH+H2O HCOO-+H3O+ HCOO-+H3O+ | B.HS-+H2O S2-+H3O+ S2-+H3O+ |
C.CO2+H2O HCO3-+H+ HCO3-+H+ | D.CO32-+H2O HCO3-+OH- HCO3-+OH- |
25℃,向一定体积0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中c(H+)与c(OH—)的变化关系如图所示,则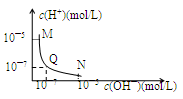
| A.M点所示溶液的导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO―)>c(Na+) |
| C.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
| D.M点和N点所示溶液中H2O的电离程度相同 |