在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是 ,
| A.pH=3的硝酸和pH=11的氢氧化钠溶液 |
| B.pH=3的盐酸和pH=11的氨水 |
| C.pH=3的硫酸和pH=11的氢氧化钠溶液 |
| D.pH=3的醋酸和pH=11的氢氧化钠溶液 |
等物质量浓度的HCN溶液与NaCN溶液等体积混合,混合液显碱性,下列说法错误的
| A.c(CN—) >c(Na+)>c(H+)>c(OH-) |
| B.c(Na+)>c(CN—)>c(OH-)>c(H+) |
| C.c(Na+)+ c(H+)= c(CN—)+ c(OH—) |
| D.2c(OH—)+ c(CN—)=2c(H+)+c(HCN) |
下列方程式中属于水解反应的是
A.HCO3-+H2O  H3O++CO32- H3O++CO32- |
B.HCO3-+H2O  OH-+H2CO3 OH-+H2CO3 |
C.NH3+H2O  NH4++OH- NH4++OH- |
| D.HCO3-+OH- =CO32-+H2O |
为除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入的一种试剂是
| A.NaOH | B.Na2CO3 | C.氨水 | D.MgO |
用食用白醋(醋酸浓度约1mol?L-1)进行下列实验,能证明醋酸为弱电解质的是
| A.白醋中滴入石蕊试液呈红色 |
| B.白醋能溶解氢氧化铜 |
| C.蛋壳浸泡在白醋中有气体放出 |
| D.pH试纸显示白醋的pH为2.3 |
50 ℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )。
| A.pH=4的醋酸中:c(H+)=4.0 mol·L-1 |
| B.饱和小苏打溶液中:c(Na+)=c(HCO3—) |
| C.饱和食盐水中:c(Na+)+c(H+)=c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2 mol·L-1 |
下列说法正确的是( )。
A.0.1 mol·L-1的醋酸溶液加水稀释, 减小 减小 |
| B.体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量),后者用时少 |
| C.向水中加入少量固体硫酸氢钠,c(H+)增大,KW变大 |
| D.常温下,V1 L pH=11的NaOH溶液与V2 L pH=3的HA溶液混合,若混合液显中性,则V1≤V2 |
下列溶液一定呈中性的是 ( )。
| A.c(H+)=c(OH-)=10-6 mol·L-1的溶液 |
| B.pH=7的溶液 |
| C.使石蕊试液呈紫色的溶液 |
| D.酸与碱恰好完全反应生成正盐的溶液 |
pH=2的两种一元酸X和Y,体积均为100 mL,稀释过程中pH与溶液体积的关系如图所示.分别滴加0.1 mol/L NaOH至pH=7,消耗NaOH溶液的体积为Vx、Vy,下列说法正确的是
A.X为弱酸,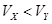 | B.Y为强酸,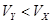 |
C.X为强酸, | D.Y为弱酸, |
