某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
| A.该温度高于25°C |
| B.由水电离出来的H+的浓度是1.0×10-10 mol/L |
| C.加入NaHSO4晶体抑制了水的电离 |
| D.该温度下加入等体积pH=12的NaOH溶液可使该溶液恰好呈中性 |
能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是 ( )
①将水加热煮沸 ②向水中投入一小块金属钠 ③向水中通CO2 ④向水中加入NH4Cl固体 ⑤向水中加入NaHCO3固体 ⑥向水中加入NaHSO4固体
| A.①②⑤ | B.①④ | C.③④⑥ | D.④ |
下列说法正确的是 ( )
| A.0.1 mol·L-1的醋酸加水稀释,c(H+)/c(OH-)减小 |
| B.体积相同、pH相同的醋酸和盐酸完全溶解等量的镁粉,后者用时少 |
| C.向水中加入少量固体硫酸氢钠,c(H+)增大,KW变大 |
| D.V1 L pH=11的NaOH溶液与V2 L pH=3的HA溶液混合,若混合液显中性,则V1≤V2 |
对滴有酚酞试液的下列溶液,操作后颜色变深的是 ( )
| A.AlCl3溶液中再溶入AlCl3 |
| B.CH3COONa溶液加热 |
| C.氨水中加入少量NH4Cl固体 |
| D.醋酸溶液加热 |
下列操作中,能使电离平衡H2O H++OH-向右移动且溶液呈酸性的是( )
H++OH-向右移动且溶液呈酸性的是( )
| A.向水中加入NaHSO4溶液 |
| B.向水中加入Al2(SO4)3溶液 |
| C.向水中加入Na2CO3溶液 |
| D.将水加热到100°C,使pH=6 |
室温下,有关下列四种溶液的叙述正确的是(忽略溶液混合后的体积变化)( )
| 序号 | ① | ② | ③ | ④ |
| pH | 12 | 12 | 2 | 2 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.在①、②中分别加入氯化铵晶体,两溶液的pH均增大
B.分别将等体积的①和②加水稀释100倍,所得溶液的pH:①>②
C.把①、④两溶液等体积混合后所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.将溶液②和溶液③等体积混合,混合后所得溶液pH=7
常温下0.1 mol·L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
| A.将溶液稀释到原体积的 10倍 |
| B.加入适量的醋酸钠固体 |
| C.加入等体积0.2 mol·L-1盐酸 |
| D.提高溶液的温度 |
下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
| | A | B | C | D |
| 强电解质 | Fe | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | H3PO4 | Fe(OH)3 |
| 非电解质 | C12H22O11(蔗糖) | BaSO4 | C2H5OH | H2O |
下列溶液中微粒的物质的量浓度关系一定正确的是( )
| A.某二元弱酸的酸式盐NaHA溶液中:c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-) |
| B.0.2 mol/L NH4Cl溶液和 0.1 mol/L NaOH溶液等体积混合:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+) |
| D.25℃时,pH=8的CH3COONa稀溶液中:c(CH3COOH)=9.9×10-7 mol/L |
在温度相同、浓度相同的条件下,下列六种物质的水溶液的pH由小到大的排列顺序如图所示。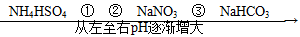
图中①②③可能是( )
| A.NH4NO3、(NH4)2SO4、CH3COONa |
| B.(NH4)2SO4、NH4Cl、C6H5ONa |
| C.(NH4)2SO4、NH4NO3、Na2CO3 |
| D.(NH4)2SO4、NH4NO3、CH3COONa |