题目内容
在温度相同、浓度相同的条件下,下列六种物质的水溶液的pH由小到大的排列顺序如图所示。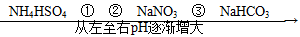
图中①②③可能是( )
| A.NH4NO3、(NH4)2SO4、CH3COONa |
| B.(NH4)2SO4、NH4Cl、C6H5ONa |
| C.(NH4)2SO4、NH4NO3、Na2CO3 |
| D.(NH4)2SO4、NH4NO3、CH3COONa |
D
解析

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
能说明醋酸是弱电解质的是
| A.中和10mL 1mol/L CH3COOH溶液需要10ml 1mol/L NaOH溶液 |
| B.用食醋可以除热水瓶内的水垢 |
| C.pH=2的醋酸溶液稀释1000倍后pH小于5 |
| D.用浓H2SO4和醋酸钠固体共热可制得醋酸 |
下列能正确表示水解的离子方程式是
A.CH3COOH + H2O 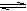 CH3COO- + H3O+ CH3COO- + H3O+ |
B.NH4+ + H2O 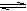 NH3·H2O + H+ NH3·H2O + H+ |
C.CO32- + 2H2O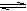 H2CO3 + 2OH- H2CO3 + 2OH- |
D.Br- + H2O 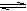 HBr + OH- HBr + OH- |
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH( pOH=-lgc(OH-) )与pH的变化关系如图所示,则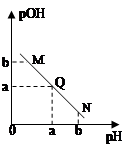
| A.N点所示溶液中c(H+) < c(OH-) |
| B.M点所示溶液导电能力强于Q点 |
| C.M点水的电离程度大于N点 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
下列关于电解质溶液的叙述正确的是( )
A.常温下,由0.1 mol·L-1一元碱BOH溶液的pH=10,可推知BOH溶液存在:BOH B++OH- B++OH- |
| B.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
| C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D.将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
为了使FeCl3溶液中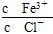 增大,可加入的物质是( )
增大,可加入的物质是( )
| A.适量的HCl气体 | B.适量的硫酸氢钠 |
| C.适量的NaOH固体 | D.适量的NaHCO3溶液 |
向含有H2SO4的CuSO4溶液中逐滴加入含a mol溶质的NaOH溶液,恰好使溶液的pH=7,下列叙述错误的是 ( )
| A.反应后溶液中c(Na+)=2c(SO42—) |
| B.a/2mol>沉淀的物质的量>0 |
| C.沉淀的质量=49a g |
| D.溶液中n(SO42—)=a/2 mol |
下列操作中,能使电离平衡H2O H++OH-向右移动且溶液呈酸性的是( )
H++OH-向右移动且溶液呈酸性的是( )
| A.向水中加入NaHSO4溶液 |
| B.向水中加入Al2(SO4)3溶液 |
| C.向水中加入Na2CO3溶液 |
| D.将水加热到100°C,使pH=6 |