将氯化铝溶液蒸干并灼烧后得到纯净的固体A,将A在高温下熔融后用铂电极进行电解,下列有关电极产物的判断正确的是
| A.阴极产物是氢气 | B.阳极产物是氧气 |
| C.阴极产物是铝和氧气 | D.阳极产物只有氯气 |
已知:25℃时,Ka(HAc)=1.7×10-5 mol /L。现有如下溶液:
①0.1mol/LHAc与0.1mol/LNaOH溶液等体积混合液
②pH = 3的HAc与pH = 11的NaOH溶液等体积混合液
③0.1 mol /LH2SO4与0.2mol/LNaOH溶液等体积混合液
常温时,三者pH大小关系正确的是
| A.①>③>② | B.③>①>② | C.①>②>③ | D.②>③>① |
下列溶液一定显酸性的是
| A.含H+的溶液 |
| B.c(OH-)<c(H+)的溶液 |
| C.pH<7的溶液 |
| D.能与金属Al反应放出H2的溶液 |
下列溶液中,粒子浓度关系正确的是
| A.0.1mol/L的Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| B.醋酸钠溶液与盐酸混合之后的中性溶液:c(Na+)> c(Cl-) >c(CH3COOH) |
| C.等浓度、等体积的氨水与盐酸的混合溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D.pH=4的NaHSO3溶液中:c(HSO3-)>c(SO32-)>c(H2SO3) |
实验:① 将0.1 mol·L-1 MgCl2溶液和0.5 mol·L-1NaOH溶液等体积混合得到浊液;
② 取少量①中浊液,滴加0.1 mol·L-1FeCl3溶液,出现红褐色沉淀;
③ 将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1FeCl3溶液,白色沉淀变为红褐色;
④ 另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解。
下列说法中,不正确的是:
| A.将①中所得浊液过滤,所得滤液中含少量Mg2+ |
B.浊液中存在溶解平衡:Mg(OH)2(s)  Mg2+(aq) + 2OH-(aq) Mg2+(aq) + 2OH-(aq) |
| C.实验②和③均能说明Fe(OH)3比Mg(OH)2难溶 |
| D.NH4Cl溶液中的NH4+可能是④中沉淀溶解的原因 |
锅炉水垢是一种安全隐患,除去水垢中的CaSO4,可先用Na2CO3溶液处理,使之转化为易溶于酸的CaCO3,而后用酸除去。下列说法不正确的是:
| A.CaCO3的溶解度小于CaSO4 |
| B.沉淀转化的实质是沉淀溶解平衡的移动 |
| C.沉淀转化的难易与溶解度差别的大小无关 |
| D.CaSO4到CaCO3的沉淀转化中并存着两个沉淀溶解平衡 |
关于室温下下列溶液的说法不正确的是
| A.水的电离程度:①=②=③=④ |
| B.分别加水稀释10倍,溶液的pH:①>②>③>④ |
C.①、③两溶液等体积混合: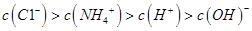 |
D.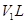 溶液②与 溶液②与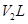 溶液③混合,若 溶液③混合,若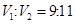 ,则混合溶液pH=4(忽略溶液体积变化) ,则混合溶液pH=4(忽略溶液体积变化) |
常温下,向等体积、等物质的量浓度的盐酸、醋酸溶液中分别滴入0.1 mol·L-1 NaOH溶液,测得溶液的pH与NaOH溶液体积的关系如图所示。下列说法错误的是( )
| A.图中曲线①表示NaOH溶液滴定盐酸时的pH变化 |
| B.酸溶液的体积均为10 mL |
| C.a点:c(CH3COOH)>c(CH3COO-) |
| D.a点:c(H+)+c(Na+)=c(OH-)+c(CH3COO-) |
常温下,向100 mL 0.1 mol·L-1 H2A(二元酸)溶液中逐滴加入0.2 mol·L-1 NaOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。下列有关说法正确的是( )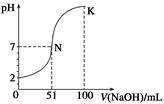
| A.H2A为二元强酸 |
| B.N点对应溶液有:c(Na+)=c(A2-)+c(HA-) |
| C.K点对应溶液中离子浓度由大到小的顺序为c(A2-)>c(Na+)>c(OH-)>c(H+) |
| D.K点时加水稀释溶液,c(H+)增大 |