现有pH=5的CH3COOH溶液10 mL,要使其pH增大3,可采取的方法有( )
| A.向溶液中加水稀释至10 L |
| B.加入一定量的NaOH固体 |
| C.加入一定量pH=8的NaOH溶液 |
| D.加入一定浓度的盐酸 |
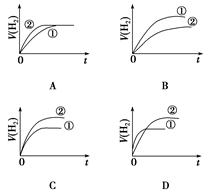
测得醋酸甲的pH:a,醋酸乙的pH:a+1。下列推断中正确的是( )
| A.醋酸甲中H+的物质的量是醋酸乙中的10倍 |
| B.醋酸乙的电离程度比醋酸甲大 |
| C.中和等物质的量的NaOH溶液需甲、乙两酸的体积之比为10∶1 |
| D.甲、乙溶液加水稀释,当pH相等时甲需加更多的水 |
下面是有关弱酸的电离平衡常数。
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 (25 ℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
结合数据,分析下列有关说法,其中错误的是( )
A.1 mol·L-1的溶液中,pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.升高温度,HCN溶液中H+浓度增大,平衡正向移动,电离平衡常数增大
C.向稀醋酸中逐滴加水,或加入少量冰醋酸,CH3COOH的电离平衡都正向移动
D.向CH3COOH溶液中加入少量氢氧化钠固体,平衡正向移动
一定温度下,向0.1 mol·L-1 CH3COOH溶液中加少量水,下列有关说法错误的是( )
| A.溶液中所有离子的浓度都减小 |
| B.CH3COOH的电离程度变大 |
| C.水的电离程度变大 |
| D.溶液的pH增大 |
H2O2是一种二元弱酸,对于0.1 mol·L-1的过氧化氢溶液,下列叙述不正确的是( )
A.H2O2的电离方程式可写作H2O2 H++HO2-,HO2- H++HO2-,HO2- H++O42- H++O42- |
| B.加水稀释过程中,K1(H2O2)增大,α(H2O2)增大,c(H+)增大 |
| C.加入少量浓盐酸,过氧化氢的电离平衡逆向移动,水的电离平衡逆向移动 |
| D.加入少量氯化铁溶液,溶液中产生大量气泡 |
甲酸的下列性质中,可以证明它是弱电解质的是( )
| A.1 mol/L甲酸溶液的c(H+)=0.01 mol/L |
| B.甲酸能与水以任何比例互溶 |
| C.10 mL 1 mol/L甲酸恰好与10 mL 1 mol/L NaOH溶液完全反应 |
| D.甲酸溶液的导电性比盐酸的弱 |
某化学兴趣小组在家中进行化学实验,按照图甲连接好线路发现灯泡不亮,按照图乙连接好线路发现灯泡亮,由此得出的结论正确的是( )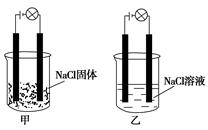
| A.NaCl是非电解质 |
| B.NaCl溶液是电解质 |
| C.NaCl是弱电解质 |
| D.NaCl在水溶液中电离出了可以自由移动的离子 |
H2SO3是二元弱酸,NaHSO3溶液呈酸性。在0.1 mol·L-1 NaHSO3溶液中,下列关系正确的是( )
| A.c(HSO3-)>c(SO32-)>c(H2SO3) |
| B.c(Na+)=c(HSO3-)+2c(SO32-)+c(H2SO3) |
| C.c(Na+)=c(HSO3-)>c(H+)>c(OH-) |
| D.c(Na+)+c(H+)=c(HSO3-)+c(OH-)+c(SO32-) |