已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH值:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
下列说法或表达中,正确的是
A.少量二氧化碳通入NaClO溶液中:2NaClO + CO2 + H2O
 Na2CO3 + 2HClO
Na2CO3 + 2HClOB.过量的HCN滴入碳酸钠溶液中HCN + Na2CO3
 NaCN+ NaHCO3
NaCN+ NaHCO3C.结合质子能力由强到弱的顺序为:CO32—>CN—>HCO3—>CH3COO—
D.常温下电离常数:Ki2(H2CO3)>Ki(C6H5OH)>Ki(HCN)
下列说法中,正确的是
| A.已知25℃时NH4CN水溶液显碱性,则25℃时的电离常数K(NH3·H2O)>K(HCN) |
| B.25℃时,Mg(OH)2固体在20 mL0.01 mol·L-1氨水中的Ksp比在20 mL0.01 mol·L-1NH4Cl溶液中的Ksp小 |
| C.pH试纸测得新制氯水的pH为4.5 |
| D.FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
实验:①0.1 mol·L-1 MgCl2溶液和0.2 mol·L-1NaOH溶液等体积混合得到浊液a,取少量浊液a过滤得到滤液b和白色沉淀c;②向浊液a中滴加0.1 mol·L-1FeCl3溶液,出现红褐色沉淀。
下列分析不正确的是
| A.滤液b的pH=7 |
| B.②中颜色变化说明Mg(OH)2转化为Fe(OH)3 |
| C.实验可以证明Fe(OH)3的溶解度比Mg(OH)2的小 |
D.浊液a中存在沉淀溶解平衡:Mg(OH)2(s) Mg2+(aq)+ 2OH-(aq) Mg2+(aq)+ 2OH-(aq) |
下列说法正确的是
| A.KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| B.25℃时、用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH |
| C.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D.AgCl易转化为AgI沉淀且K(AgX)=c(Ag+)? c(X—),故K(AgI)<K(AgCl) |
下列有关溶度积常数Ksp的说法正确的是
| A.常温下,向BaCO3饱和溶液中加入Na2CO3固体,BaCO3的Ksp减小 |
| B.溶度积常数Ksp只受温度影响,温度升高Ksp减小 |
| C.溶度积常数Ksp只受温度影响,温度升高Ksp增大 |
| D.常温下,向Mg(OH)2饱和溶液中加入NaOH固体,Mg(OH)2的Ksp不变 |
在25 ℃时,FeS的Ksp=6.3×10-18,CuS的Ksp=1.3×10-36,ZnS的Ksp=1.3×10-24。下列有关说法中正确的是
| A.25 ℃时,CuS的溶解度大于ZnS的溶解度 |
| B.25 ℃时,饱和CuS溶液中Cu2+的浓度为1.3×10-36 mol·L-1 |
| C.向物质的量浓度相同的FeCl2、ZnCl2的混合液中加入少量Na2S,只有FeS沉淀生成 |
| D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂 |
已知25℃,Fe(OH)3(s) Fe3+(aq)+3OH-(aq),Ksp;Fe3++3H2O
Fe3+(aq)+3OH-(aq),Ksp;Fe3++3H2O Fe(OH)3+3H+,Kh;水的离子积常数为Kw。下列Ksp、Kh、Kw的关系是
Fe(OH)3+3H+,Kh;水的离子积常数为Kw。下列Ksp、Kh、Kw的关系是
| A.Ksp·Kh=Kw3 | B.Ksp·Kw=Kh |
| C.Kh/Kw=Ksp | D.Kw/Kh=Ksp3 |
已知25 ℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100 mL该条件下的CaSO4饱和溶液中加入400 mL 0.01 mol·L-1 Na2SO4溶液,下列叙述正确的是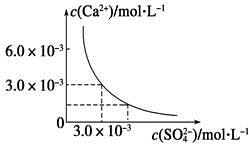
| A.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)比原来的大 |
| B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小 |
| C.溶液中析出CaSO4固体沉淀,溶液中c(Ca2+)、c(SO42-)都变小 |
| D.溶液中无沉淀析出,但最终溶液中c(SO42-)比原来的大 |
相同温度下,在水中分别加入下列物质,若用Kw表示水的离子积,a表示水的电离程度,能使a/Kw的值增大的是
| A.NaOH | B.NaHSO4 | C.HC1 | D.NH4NO3 |
250C时,pH=3的HNO3,下列该硝酸说法正确的是
| A.该硝酸中水电离出的c(H+)=1.0×10-3mol/L |
| B.加水稀释到原溶液体积的100倍,硝酸溶液的pH为5 |
| C.相同温度下,pH=3的CH3COOH溶液的物质的量浓度与该硝酸相同 |
| D.该硝酸中加入少量的Zn粒产生H2 |