下图表示的是某物质所发生的( )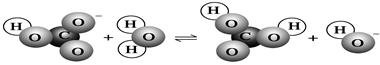
| A.取代反应 | B.水解反应 |
| C.中和反应 | D.电离过程 |
对于常温下pH=2的盐酸和pH=3的醋酸,下列说法正确的是
| A.pH=2的盐酸中:c(H+)=c(Cl-) + c(OH-) |
| B.pH=3的醋酸中:c(H+)=3.0 mol·L-1 |
| C.pH=2的盐酸与pH=3的醋酸中溶质的物质的量浓度之比为10:1 |
| D.pH=3的醋酸与pH=11的NaOH溶液等体积混合所得溶液中:c(Na+)=c(CH3COO-) |
下列说法正确的是 ( )
| A.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
| B.因为CH3COOH是弱电解质,HCl是强电解质,所以中和等体积等物质的量浓度的醋酸和盐酸时,中和醋酸消耗的NaOH比盐酸消耗的NaOH用量少 |
| C.物质的量浓度相同的磷酸钠溶液和磷酸溶液中PO43-的物质的量浓度相同 |
| D.足量Zn分别和等体积、等物质的量浓度的盐酸和醋酸反应时,产生H2的量相同,放出H2的速率不等 |
常温下,把pH=3的H2SO4溶液和pH=10的NaOH溶液混合,两者恰好中和,则酸和碱的体积比应是
| A.10∶1 | B.1∶10 | C.1∶100 | D.1∶2 |
下列各溶液中,相关微粒物质的量浓度关系不正确的是
| A.0.1 mol·L-1NaHCO3溶液中:c(OH-)=c(H+)+c(H2CO3)-c(CO32-) |
| B.0.1 mol·L-1NH4Cl溶液中:c(Cl-)=c(NH4+)+c(NH3·H2O)=0.1 mol·L-1 |
| C.pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+)+c(M+)=c(OH-)+c(A-) |
| D.常温下,浓度为0.1 mol·L-1 NaHSO3溶液的pH<7:c(Na+)>c(HSO3-)>c(SO32-)> c(H+) |
下列有关溶液的叙述中,正确的是
| A.中和10 mL 0.1 mol·L-1醋酸与中和100 mL 0.01 mol·L-1的醋酸所需同种碱溶液的量不同 |
| B.常温下,等体积的pH=3的酸溶液和pH=11的碱溶液混合,混合后溶液的pH=7 |
| C.常温下,体积相等、pH相同的盐酸和硫酸溶液,两溶液溶质的物质的量浓度相等 |
| D.常温下,pH=3的甲酸溶液的c(H+)与pH=11的氨水溶液的c(OH-)相等 |
若醋酸用HAc表示,则在0.1mol·L-1 NaAc溶液中,下列离子浓度关系正确的是
| A.c(Na+)= c(Ac—)+c(HAc) |
| B.c(Na+)+c(OH—)= c(Ac—)+c(H+) |
| C.c(Na+)>c(OH—) > c(Ac—) > c(H+) |
| D.c(Na+)> c(Ac—)> c(H+)> c(OH—) |
下列表述中,合理的是
| A.将水加热,Kw增大,pH不变 |
| B.把FeCl3的水溶液加热蒸干可得到FeCl3固体 |
| C.用25 mL碱式滴定管量取20.00mL高锰酸钾溶液 |
| D.用惰性电极电解足量的AgNO3溶液时,当有0.2 mole-转移时会析出21.6g银 |
在室温下,下列叙述正确的是
A.将 的一元酸溶液稀释到 的一元酸溶液稀释到 ,若溶液的 ,若溶液的 ,则此酸为弱酸 ,则此酸为弱酸 |
B.将  盐酸稀释到 盐酸稀释到 ,得到 ,得到 的盐酸 的盐酸 |
C.用 的盐酸分别中和 的盐酸分别中和 溶液和氨水, 溶液和氨水,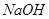 消耗盐酸的体积大 消耗盐酸的体积大 |
D. 的盐酸与 的盐酸与 的硫酸比较, 的硫酸比较, |
25℃时,水中存在电离平衡:

 。下列叙述正确的是
。下列叙述正确的是
A.将水加热, 增大, 增大, 不变 不变 |
B.向水中加入少量NaHSO4固体,c(H+)增大, 不变 不变 |
C.向水中加入少量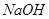 固体,平衡逆向移动, 固体,平衡逆向移动, 降低 降低 |
D.向水中加入少量 固体,平衡正向移动, 固体,平衡正向移动, 增大 增大 |