将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)  2HBr(g)△H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
2HBr(g)△H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
| A.a>b | B.a=b | C.a<b | D.无法确定 |
在一个固定容积的密闭容器中充入2molNO2,一定温度下建立如下平衡:2NO2 N2O4,此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是( )
N2O4,此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是( )
| A.x>y | B.x<y | C.x=y | D.不能确定 |
可逆反应∶2NO2 2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2的同时,生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥ 混合气体的平均相对分子质量不再改变的状态
| A.①④⑥ | B.②③⑤ | C.①③④ | D.①②③④⑤ |
在一固定体积的密闭容器中加入2 mol A和1 mol B发生反应2A(g)+B(g) 3C(g)+D(g),达到平衡时C的浓度为w mol·L-1,若维持容器的体积和温度不变,按下列四种配比方案作为反应物,达平衡后,使C的浓度仍为w mol·L-1的配比是( )
3C(g)+D(g),达到平衡时C的浓度为w mol·L-1,若维持容器的体积和温度不变,按下列四种配比方案作为反应物,达平衡后,使C的浓度仍为w mol·L-1的配比是( )
| A.4 mol A+2 mol B | B.3 mol C+1 mol D+2mol A+1 mol B |
| C.3mol C+1 mol D+1 mol B | D.3 mol C+1 mol D |
对下列图像的描述正确的是( )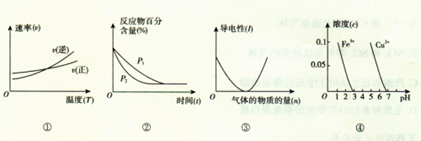
A.根据图①可判断反应A2(g)+3B2(g)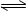 2AB3(g)的△H>0 2AB3(g)的△H>0 |
B.图②可表示压强(P)对反应2A(g)+2B(g)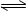 3C(g)+D(s)的影响 3C(g)+D(s)的影响 |
| C.图③可表示向醋酸溶液通人氨气时,溶液导电性随氨气量的变化 |
| D.根据图④,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 |
在一定温度下,将两种气体M和N通入容积为V L的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示,下列说法不正确的是 ( )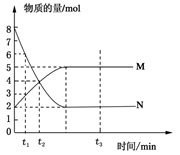
| A.t2时M与N的物质的量浓度之比为1:1 |
| B.t2与t3时刻的混合气体的平均相对分子质量相等 |
| C.反应物与生成物平衡时的物质的量浓度之比是2:5 |
D.0~t2内用M表示的平均反应速率是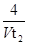 mol/(L?min) mol/(L?min) |
工业生产硫酸时,其中一步反应是2SO2 + O2 2SO3,该反应正反应是放热反应,下列说法不正确的是( )
2SO3,该反应正反应是放热反应,下列说法不正确的是( )
| A.升高温度可提高反应速率 |
| B.使用催化剂能增大反应速率 |
| C.增大氧气浓度可提高SO2的转化率 |
| D.达到化学平衡时正逆反应速率相等且都为零 |
在同温同压条件下,已知: C+CO2 2CO(正反应是吸热),正反应的反应速率为v1;N2+3H2
2CO(正反应是吸热),正反应的反应速率为v1;N2+3H2 2NH3(正反应是放热),正反应的反应速率为v2。对于上述反应,当温度同时升高时,v1和v2的变化情况正确的是
2NH3(正反应是放热),正反应的反应速率为v2。对于上述反应,当温度同时升高时,v1和v2的变化情况正确的是
| A.同时增大 | B.同时减小 |
| C.v1增大,v2减小 | D.v1减小,v2增大 |
反应2SO2+O2 2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
| A.0.1s | B.2.5s | C.5s | D.10s |
 2AB(g)达到平衡的标志是( )
2AB(g)达到平衡的标志是( )