在容积恒定的密闭容器中,一定量的SO2与1.1molO2发生反应: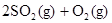
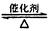
 。当气体的物质的量减少0.315mol时,反应达到平衡,SO2的平衡转化率是90%。下列说法正确的是
。当气体的物质的量减少0.315mol时,反应达到平衡,SO2的平衡转化率是90%。下列说法正确的是
| A.相同条件下,平衡时若充入稀有气体,SO2的转化率增大 |
| B.反应开始时,向容器中通入的SO2的物质的量是0.7mol |
| C.保持其他条件不变,仅降低温度,正反应速率减小程度比逆反应速率减小程度大 |
| D.保持其他条件不变,仅缩小容器体积,反应达到平衡时容器中有1.485mol气体 |
在容积相同的五个密闭容器中分别放入等量的A2和B2,在不同温度下同时任其发生反应:A2(g)+3B2(g) 2AB3(g),分别在某一同时刻测得其中AB3所占的体积分数变化如图所示,下列说法不正确的是
2AB3(g),分别在某一同时刻测得其中AB3所占的体积分数变化如图所示,下列说法不正确的是
| A.正反应是放热反应 | B.E、F二点尚未达到平衡 |
| C.H、I二点尚未达到平衡 | D.G、H、I三点已达平衡状态 |
某温度下,某容积恒定的密闭容器中发生如下可逆反应:
CO(g)+H2O(g) H2(g)+CO2(g)△H>0。当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
H2(g)+CO2(g)△H>0。当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
| A.升高温度 | B.加入催化剂 |
| C.再加入n molCO和n molH2O | D.再加入2n molCO2和2n molH2 |
已知反应2CH3OH(g) CH3OCH3(g)+H2O(g)。某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)。某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/mol·L-1 | 0.44 | 0.6 | 0.6 |
下列叙述中正确的是
A.该反应的平衡常数表达式为K=[c(CH3OCH3)×c(H2O)]/c(CH3OH)
B.此时正、逆反应速率的大小:υ正<υ逆
C.若经10min后反应达到平衡,此时c(CH3OH)=0.04mol/( L·min)
D.0~10min内平均反应速率υ(CH3OH)=1.6mol/(L·min)
可逆反应aA(g)+bB(g) cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是
cC(g)+dD(s);△H=QkJ·mol-1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、反应速率(v)与压强的关系如图所示。据图分析,以下说法正确的是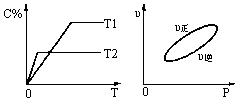
| A.T1<T2,Q>0 |
| B.增大压强,B的转化率减小 |
| C.当反应达平衡时,混合气体的密度不再变化 |
| D.a+b>c+d |
某密闭容器中发生如下反应 X(g)+3Y(g) 2Z(g)ΔH<0。该反应的速率(v)随时间(t)变化的关系如下图所示,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。则下列说法中错误的是
2Z(g)ΔH<0。该反应的速率(v)随时间(t)变化的关系如下图所示,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。则下列说法中错误的是
| A.t2时加入了催化剂 |
| B.t3时减小了体系压强 |
| C.t5时升高了体系温度 |
| D.t2、t3、t5变化后反应物转化率均比t1时减小 |
一定温度下,可逆反应 A2(g)+3B2(g)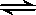 2AB3(g) 达到平衡的标志是
2AB3(g) 达到平衡的标志是
| A.容器内每减少1mol A2,同时生成2mol AB3 |
| B.容器内每减少1mol A2,同时生成3mol B2 |
| C.容器内A2、B2、AB3的物质的量之比为1:3:2 |
| D.容器内A2、B2、AB3的物质的量浓度相等 |
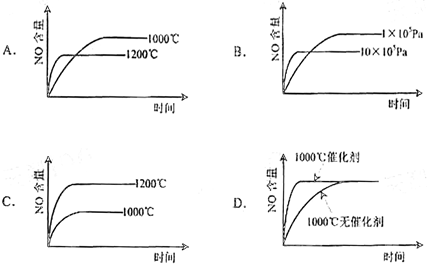
已知在某密闭容器中发生反应 4NH3+5O2=4NO+6H2O,若反应速率分别用
υ(NH3)、υ(O2)、υ(NO)、υ(H2O)表示,则下列关系正确的是
A.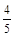 υ(NH3) =υ(O2) υ(NH3) =υ(O2) | B.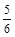 υ(O2) =υ(H2O) υ(O2) =υ(H2O) |
C.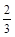 υ(NH3) =υ(H2O) υ(NH3) =υ(H2O) | D.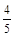 υ(O2) =υ(NO) υ(O2) =υ(NO) |