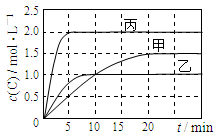
一定条件下,Cu2+、Mn2+、Fe3+的浓度对乙酸在光照下催化降解速率的影响如图所示。下列判断错误的是
| A.该实验方案的缺陷之一是未做空白对照实验 |
| B.Cu2+、Mn2+提高乙酸降解速率的最佳浓度为0.1 mmol·L-l |
| C.Fe3+不能提高乙酸降解速率 |
| D.相同条件下,乙酸在Cu2+、Mn2+、Fe3+作用下的降解速率依次减小 |
如图是可逆反应X2+3Y2 2Z2在反应过程中的反应速率V与时间(t)的关系曲线,下
2Z2在反应过程中的反应速率V与时间(t)的关系曲线,下
列叙述正确的是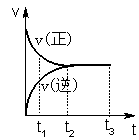
| A.t1时,只有正方向反应 |
| B.t2时,反应到达限度 |
| C.t2-t3,反应不再发生 |
| D.t2-t3,X2、Y2、Z2的物质的量浓度之比为1∶3∶2 |
反应C(s)+H2O(g) CO(g)+H2(g)在一恒容密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一恒容密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
| A.通入水蒸气 | B.升温 | C.加入催化剂 | D.充入He |
用铁片与0.1mol/L硫酸反应制氢气时,下列措施不能使氢气生成速率加大的是
| A.改用98%浓硫酸 | B.加热 |
| C.改用2mol/L硫酸 | D.把铁片换成铁粉 |
可逆反应N2 (g)+3H2(g)  2NH3(g) △H<0,下列研究目的和示意图相符的是( )
2NH3(g) △H<0,下列研究目的和示意图相符的是( )
| | A | B | C | D |
| 研究 目的 | 压强对反应的影响 (p2>p1) | 温度对反应的影响 | 平衡体系增加N2的 浓度对反应的影响 | 催化剂对反应的影响 |
| 图 |  |  |  |  |
一定温度下,l mol X和n mol Y在体积为2L的密闭容器中发生如下反应:X(g) + Y(g) 2Z(g) + M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
2Z(g) + M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
| A.用X表示5min内此反应的反应速率是(0.1—0.2a)mol·(L·min)—1 |
| B.当混合气体的质量不再发生变化时,说明反应达到平衡状态 |
| C.向平衡后的体系中加入l mol M,平衡向逆反应方向移动 |
| D.向上述平衡体系中再充入l mol X,v(正)增大,v(逆)减小,平衡正向移动 |
某容积可变的密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+B(g) 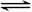 2C(g)+Q(Q>0),容器中物质浓度随时间变化的曲线如图所示。下列说法中正确的是
2C(g)+Q(Q>0),容器中物质浓度随时间变化的曲线如图所示。下列说法中正确的是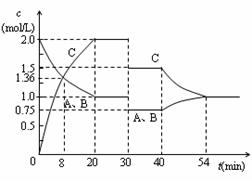
| A.30min时降低温度,40min时升高温度 |
| B.40min~54min之间反应速率v(正) < v(逆) |
| C.设20min和30min时的平衡常数分别为K1和K2,则K1 >K2 |
| D.0~8minA的平均反应速率为0.64mol/(L·min) |
实验室用锌粒与VmL浓度为10%的稀硫酸反应制取氢气,若向反应混合物中加入下列物质,关于反应速率v说法正确的是
| A.少量Na2SO4固体,v(H2)减小 | B.VmLBaCl2溶液,v(H2)不变 |
| C.加入细小的碳粒,v(H2)增大 | D.加入NH4HSO4固体,v(H2)不变 |
 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和下图表示: