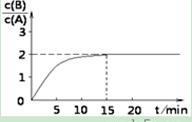
在四个不同的容器中,在不同的条件下进行合成氨反应。根据在相同时间呢测定的结果判断,生成氨的速率最快的是( )
| A.v(H2) =0.1mol?L-1?min-1 | B.v(N2)=0.2mol?L-1?min-1 |
| C.v(NH3)=0.15mol?L-1?min-1 | D.v(H2)=0.3mol?L-1?min-1 |
对已经达到化学平衡的2X(g)+Y(g) 2Z(g)减小压强时,对反应的影响是( )
2Z(g)减小压强时,对反应的影响是( )
| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
反应2SO2(g)+O2 2SO3(g)经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s),则这段时间为( )
2SO3(g)经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s),则这段时间为( )
| A.0.1s | B.2.5s | C.10s | D.5s |
决定化学反应速率的主要因素是( )
| A.反应物的浓度 | B.反应体系内的压强 |
| C.反应物的性质 | D.反应物的状态 |
下列说法正确的是( )
| A.增大反应物的量化学反应速率一定加快 |
| B.升高温度可使放热反应速率减慢,吸热反应速率加快 |
| C.增大压强化学反应速率一定加快 |
| D.使用催化剂能加快反应速率 |
对于反应:H2(g)+I2(g) 2HI(g),在一恒定压强的容器中进行,下列可以判断此反应达到平衡状态的是( )
2HI(g),在一恒定压强的容器中进行,下列可以判断此反应达到平衡状态的是( )
| A.混合气体的体积保持不变 | B.混合气体的密度保持不变 |
| C.混合气体平均相对分子质量保持不变 | D.混合气体颜色保持不变 |
高温下,某反应达到平衡,平衡常数 。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
A.该反应的化学方程式为CO+H2O CO2+H2 CO2+H2 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,正反应速率增大,逆反应速率减小 |
| D.该反应的焓变为正值 |
可逆反应A(?)+aB(g)  C(g)+2D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列说法不正确的是
C(g)+2D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列说法不正确的是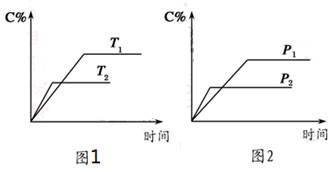
| A.若a=2,则A为液态或固体 |
| B.该反应的正反应为放热反应 |
| C.T2>T1,p2>p1 |
| D.其他条件不变,增加B的物质的量,平衡正向移动,平衡常数K增大 |
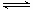 B(g) + C(g);ΔH = ?48.25 kJ/L
B(g) + C(g);ΔH = ?48.25 kJ/L