题目内容
对于反应:H2(g)+I2(g) 2HI(g),在一恒定压强的容器中进行,下列可以判断此反应达到平衡状态的是( )
2HI(g),在一恒定压强的容器中进行,下列可以判断此反应达到平衡状态的是( )
| A.混合气体的体积保持不变 | B.混合气体的密度保持不变 |
| C.混合气体平均相对分子质量保持不变 | D.混合气体颜色保持不变 |
D
解析试题分析:可逆反应平衡状态的判断依据为: (1)“双向同时,符合比例”:反应速率必须一个是正反应的速率,一个是逆反应的速率,速率用不同物质表示时,速率之比等于方程式前的系数比;(2)“变量不变,已达平衡”:如果一个量随反应的进行而改变,当它不变时达到平衡状态;一个随反应的进行保持不变的量—恒量,不能作为是否是平衡状态的判断依据。对于反应:H2(g)+I2(g) 2HI(g),反应前后气体的物质的量和质量保持不变,在一恒定压强的容器中进行,根据阿伏加德罗定律及密度和摩尔质量的定义分析知,混合气体的体积、密度、相对分子质量均为恒量,不能作为是否是平衡状态的判断依据,混合气体颜色是由碘蒸气的浓度决定的,碘蒸气的浓度在反应前后为变量,当它不变时达到平衡状态,选D.
2HI(g),反应前后气体的物质的量和质量保持不变,在一恒定压强的容器中进行,根据阿伏加德罗定律及密度和摩尔质量的定义分析知,混合气体的体积、密度、相对分子质量均为恒量,不能作为是否是平衡状态的判断依据,混合气体颜色是由碘蒸气的浓度决定的,碘蒸气的浓度在反应前后为变量,当它不变时达到平衡状态,选D.
考点:考查可逆反应平衡状态的判断。

T10C 时,将9molCO2和12molH2充入3L密闭容器中,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH <0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法正确的是
CH3OH(g)+H2O(g) ΔH <0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法正确的是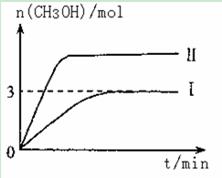
| A.曲线II对应的条件改变是减小压强 |
| B.若T2°C时上述反应的平衡常数为0.42,则T2< T1 |
| C.在T10C,若起始时向容器中充入5 mol CO2、5 mol H2、5 mol CH3OH(g)和 5 mol H2O(g),则达平衡前v(正)>v(逆) |
| D.在T10C,若起始时向容器中通入4 .5 molCO2、6mol H2 ,平衡时容器内的压强P1=P/2 |
下列说法正确的是 ( )
| A.碳酸铵分解是吸热反应,根据焓判据判断能自发分解 |
| B.多次洗牌以后,扑克牌的毫无规律的混乱排列的几率大,越混乱,熵值越大 |
| C.水总是自发地由高处往低处流,这是一个自发反应 |
| D.室温下水结成冰是自发过程 |
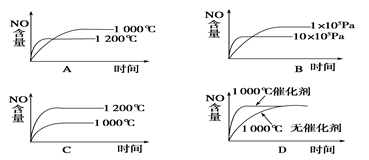
已知反应4CO(g)+2NO2(g) N2(g)+4CO2(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是
N2(g)+4CO2(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是
| A.v(CO)=1.5 mol·L-1·min-1 |
| B.v(NO2)=0.7 mol·L-1·min-1 |
| C.v(N2)=0.4 mol·L-1·min-1 |
| D.v(CO2)=1.1 mol·L-1·min-1 |
反应2SO2(g)+O2 2SO3(g)经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s),则这段时间为( )
2SO3(g)经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s),则这段时间为( )
| A.0.1s | B.2.5s | C.10s | D.5s |
在一定条件下,固定容积的密闭容器中反应:2NO2(g)  2NO(g)+O2(g)△H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
2NO(g)+O2(g)△H>0,达到平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是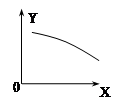
| A.X表示温度时,Y表示NO2物质的量 |
| B.X表示NO2物质的量,Y表示O2的物质的量 |
| C.X表示反应时间时,Y表示混合气体的密度 |
| D.X表示压强时,Y表示NO2的含量 |
已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) △H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是( )
N2O4(g) △H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是( )
| A.图中的两条曲线,X表示NO2浓度随时间的变化曲线 |
| B.前10 min内用v(N2O4 ) =" 0.2" mol/(L·min) |
| C.25 min时,NO2转变为N2O4的反应速率增大,其原因是将密闭容器的体积缩小为1L |
| D.前10 min内用v(NO2) =" 0.04" mol/(L·min) |
在一定条件下,已达平衡的可逆反应:2A(g)+B(g)  2C(g),下列说法中正确的是 ( )
2C(g),下列说法中正确的是 ( )
A.平衡时,此反应的平衡常数K与各物质的浓度有如下关系:K=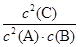 |
| B.改变条件后,该反应的平衡常数K一定不变 |
| C.如果改变压强并加入催化剂,平衡常数会随之变化 |
| D.若平衡时增加A和B的浓度,则平衡常数会减小 |