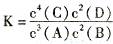I2在KI溶液中存在平衡: 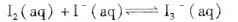 ,某I2、、KI混合溶液中, c(
,某I2、、KI混合溶液中, c(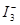 )与温度T的平衡曲线图如下。下列说法不正确的是
)与温度T的平衡曲线图如下。下列说法不正确的是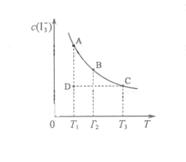
A.反应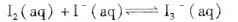 的△H>0 的△H>0 |
B.若温度为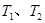 ,反应的平衡常数分别为 ,反应的平衡常数分别为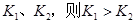 |
C.若反应进行到状态D时,一定有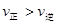 |
| D.状态A与状态B相比,状态A的c(I2) 小 |
为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究。T1℃时,将9molCO2和12molH2充入3L密闭容器中,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P1。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法错误的是( )
CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线I所示,平衡时容器内压强为P1。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线II所示。下列说法错误的是( )
| A.曲线II对应的条件改变是增大压强 |
| B.T2℃时,上述反应平衡常数为0.42,则T2>T1 |
| C.在T1℃,若起始时向容器中充入 5 mol CO2、5 mol H2、5 mol CH3OH(g)和5 mol H2O(g),则达平衡前v(正)>v(逆) |
D.在T1℃,若起始时向容器中充入4.5molCO2、6mol H2 ,平衡时容器内压强p= |
pH值相同的盐酸溶液和醋酸溶液分别和锌反应,若最后锌都已完全溶解,放出的氢气一样多,则下列判断正确的是( )
| A.整个反应阶段平均速率:醋酸>盐酸 | B.反应所需时间:醋酸>盐酸 |
| C.参加反应的锌的质量:盐酸<醋酸 | D.开始反应速率:盐酸>醋酸 |
实验室用足量铁粉与一定量的某浓度的盐酸反应来制得氢气。由于反应速率太快,不易操作。为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是( )
| A.CH3COONa固体 | B.NaOH溶液 | C.(NH4)2 SO4粉末 | D.K2 SO4固体 |
对于可逆反应H2(g) + I2(g) 2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
2HI(g),在温度一定下由H2(g)和I2(g)开始反应,下列说法正确的是( )
| A.H2(g)的消耗速率与HI(g)的生成速率比为2:1 |
| B.反应进行的净速率是正、逆反应速率之差 |
| C.正、逆反应速率的比值是恒定的 |
| D.达到平衡时,正、逆反应速率不一定相等 |
在一定条件下,向一带活塞的密闭容器中充入2mol NO2,发生下列反应2NO2(g)  N2O4(g) ΔH < 0,达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图。下列对t1时刻改变条件的推测中正确的是
N2O4(g) ΔH < 0,达到平衡状态后,在t1时刻改变条件,化学反应速率随时间变化关系如图。下列对t1时刻改变条件的推测中正确的是
| A.保持压强不变,升高反应温度 |
| B.保持温度和容器体积不变,充入1mol N2(g) |
| C.保持温度和容器体积不变,充入1mol N2O4(g) |
| D.保持温度和压强不变,充入1mol N2O4(g |
已知:2X+Y 2Z,反应中ω(Z的物质的量分数)随温度T的变化如下图所示。下列判断正确的是
2Z,反应中ω(Z的物质的量分数)随温度T的变化如下图所示。下列判断正确的是
| A.T1时,v正>v逆 |
| B.正反应的△H<0 |
| C.a、b两点的反应速率va=vb |
| D.T<T1时,ω增大的原因是平衡向正方向移动 |
大气中的SO2是造成酸雨的主要污染物。最新研究表明,[N(CH3)4]2SO4(s)能与SO2进行如下可逆反应,使其可能成为绿色的SO2吸收剂[N(CH3)4]2SO4(s)+ SO2 [N(CH3)4]2S2O6(s)ΔH<0 则用[N(CH3)4]2SO4(s)吸收SO2的适宜条件为
[N(CH3)4]2S2O6(s)ΔH<0 则用[N(CH3)4]2SO4(s)吸收SO2的适宜条件为
| A.高温高压 | B.低温高压 | C.高温低压 | D.低温低压 |
 4C(1)+2D( g)。平衡时测得n(C)="1.6mol" ,反应的化学平衡常数表达式为
4C(1)+2D( g)。平衡时测得n(C)="1.6mol" ,反应的化学平衡常数表达式为