某温度下,体积一定的密闭容器中进行可逆反应:X(g)+Y(g) Z(g)+W(s) ΔH > 0,
Z(g)+W(s) ΔH > 0,
下列叙述正确的是
| A.加入少量W,逆反应速率增大 |
| B.当容器中气体密度不变时,反应达到平衡 |
| C.升高温度,Y的百分含量减少 |
| D.平衡后加入X,上述反应的ΔH增大 |
C+CO2 2CO △H 1>0,反应速率v1 ,N2+3H2
2CO △H 1>0,反应速率v1 ,N2+3H2 2NH3 △H 2<0,反应速率v2 。若升高温度,v1和v2的变化是
2NH3 △H 2<0,反应速率v2 。若升高温度,v1和v2的变化是
| A.同时增大 | B.同时减少 | C.v1增大,v2减少 | D.v1减少,v2增大 |
一定温度下,在2L密闭容器中发生下列反应:4NO2(g)+O2(g) 2N2O5(g);已知该反应的平衡常数:
2N2O5(g);已知该反应的平衡常数: >
> ,且体系中
,且体系中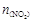 (单位:mol)随时间变化如下表:
(单位:mol)随时间变化如下表:
| 时间(s) | 0 | 500 | 1000 | 1500 |
| t1℃ | 20 | 13.96 | 10.08 | 10.08 |
| t2℃ | 20 | a | b | c |
下列说法一定正确的是( )
A.正反应为吸热反应
B.如果t2℃<t1℃,那么 a>b=c,且a=10+0.5b
C.如果t2℃<t1℃,那么t2℃达到平衡的时间介于1000s至1500s之间
D.如果t2℃>t1℃,那么b>10.08
下列有关说法正确的是 ( )
| A.合成氨反应需使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动 |
| B.常温下,将pH =10的氨水稀释,溶液中所有离子浓度都减小 |
| C.100 mL pH=3的HA和HB分别与足量的锌反应,HA放出的氢气多,说明HA酸性比HB弱 |
D.已知  I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1。恒容时, 体系中各物质浓度随时间变化的曲线如图示。下列说法不正确的是( )
2NH3(g) △H=-92.4 kJ·mol-1。恒容时, 体系中各物质浓度随时间变化的曲线如图示。下列说法不正确的是( )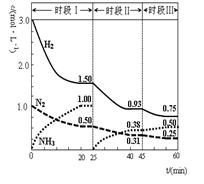
| A.前20分钟反应内放出的热量为46.2kJ |
| B.第25分钟改变的条件是将NH3从反应体系中分离出去 |
| C.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
| D.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变 |
 2C(g)(正反应吸热),下列图象正确的是
2C(g)(正反应吸热),下列图象正确的是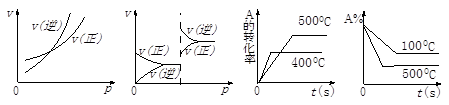
 2C(g)。若经2 s后测得C的浓度为0.6 mol/L,下列几种说法正确的是
2C(g)。若经2 s后测得C的浓度为0.6 mol/L,下列几种说法正确的是
 xC(g) △H<0测得两容器中c(A)随时间t的变化如图所示。
xC(g) △H<0测得两容器中c(A)随时间t的变化如图所示。