在一密闭容器中有如下反应:aX(g)+bY(s)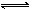 nW(g);ΔH=Q。某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:( )
nW(g);ΔH=Q。某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:( )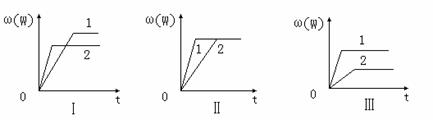
其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析正确的是( )
| A.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a<n |
| B.图Ⅱ可能是在同温同压下催化剂对反应的影响,且2使用的催化剂效果好 |
| C.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n=a+b |
| D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0 |
已知2SO2(g)+O2(g)  2SO3 (g) △H =-a kJ·mol-1(a>0)。恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,反应放出热量x kJ
2SO3 (g) △H =-a kJ·mol-1(a>0)。恒温恒容下,在10L的密闭容器中加入0.1molSO2和0.05molO2,经过2min达到平衡状态,反应放出热量x kJ
下列判断正确的是( )
| A.反应放出热量x="0.05" a |
| B.反应达到平衡状态时,2v (SO2)消耗=" v" (O2) 生成 |
| C.若恒温恒压下,在10L的密闭容器中加入0.1molSO2和0.05molO2,平衡后反应放出的热量y kJ,则y < x |
| D.升高温度,平衡常数变小 |
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的速率可表示为( )。
| A.v(NH3)=0.01 mol·L-1·s-1 | B.v(O2)=0.001 mol·L-1·s-1 |
| C.v(NO)=0.001 mol·L-1·s-1 | D.v(H2O)=0.045 mol·L-1·s-1 |
下列关于化学反应速率的说法中正确的是( )。
| A.化学反应速率可用某时刻生成物的物质的量来表示 |
| B.在同一反应中,用反应物或生成物表示的化学反应速率的值是相等的 |
| C.化学反应速率是指反应进行的时间内,反应物浓度的减少或生成物浓度的增加 |
| D.可用单位时间内氢离子物质的量浓度的变化来表示氢氧化钠和硫酸的反应速率 |
一定条件下,在密闭容器中,能表示反应X(g)+2Y(g) 2Z(g)一定达到化学平衡状态的是
2Z(g)一定达到化学平衡状态的是
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
| A.①② | B.①④ | C.②③ | D.③④ |
可逆反应2SO2+O2 2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是
2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是
①v(SO2)=v′(SO2)
②v(O2)=v′(SO2)=v(SO3)
③v(O2)= v′(SO2)
v′(SO2)
④v′(SO2)=v′(O2)=v′(SO3)
| A.①②③④ | B.①②③ | C.②③④ | D.①③ |
化学平衡常数(K)、电离常数(Ka)、溶度积常数(Ksp)是判断物质性质或变化的重要的常数。下列关于这些常数的说法中,正确的是( )
| A.化学平衡常数的大小与温度、浓度、压强、催化剂有关 |
| B.CH3COONH4溶液几乎呈中性,说明Ka(CH3COOH)与Kb(NH3·H2O)近似相等 |
| C.Ksp(AgCl)>Ksp(AgI),由此可以判断AgCl(s)+I-=AgI(s)+Cl-能够发生 |
| D.Ka(HCN)<Ka(CH3COOH),说明相同浓度时,氢氰酸的酸性比醋酸强 |
将a L NH3通过灼热的装有铁触媒的硬质玻璃管后,气体体积变为
b L(气体体积均在同温同压下测定),该b L气体中NH3的体积分数是( )
A. ×100% ×100% | B. ×100% ×100% |
C. ×100% ×100% | D. ×100% ×100% |
为探究Fe2+ 对O3氧化I-反应的影响,某研究小组测定两组实验中I3-浓度和体系pH,结果见以下图表。
下列说法不正确的是( )
A.在溶液中存在化学平衡I2(aq) + I-(aq)  I3-(aq),其平衡常数表达式为 I3-(aq),其平衡常数表达式为 |
| B.第2组实验进行18s后,由于I2(g)不断生成导致I3-浓度下降。 |
| C.3-18s内第2组实验中生成I3-的平均反应速率约为0.55 mol/(L·s) |
| D.Fe2+可作为O3氧化I-的催化剂 |
 3C+4D反应中,表示该反应速率最快的是( )。
3C+4D反应中,表示该反应速率最快的是( )。