下图是关于反应A2(g)+3B2(g) 2C(g)(正反应为放热反应)的平衡移动图像,影响平衡移动的原因可能是( )
2C(g)(正反应为放热反应)的平衡移动图像,影响平衡移动的原因可能是( )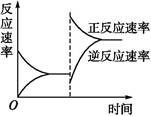
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |
合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:
CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0
CO2(g)+H2(g) ΔH<0
反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )
| A.增加压强 | B.降低温度 |
| C.增大CO的浓度 | D.更换催化剂 |
在密闭容器中进行反应:H2(g)+Br2(g) 2HBr(g) ΔH<0,达到平衡后,欲使颜色加深,应采取的措施是( )
2HBr(g) ΔH<0,达到平衡后,欲使颜色加深,应采取的措施是( )
| A.升高温度 | B.降低温度 |
| C.增大H2浓度 | D.减小压强 |
下列能确认化学平衡发生了移动的是( )
| A.化学反应速率发生改变 |
| B.有气态物质参加的可逆反应达到平衡后,改变压强 |
| C.由于某一条件的改变,使平衡体系中各组分的浓度发生了不同程度的改变 |
| D.可逆反应达到平衡后,使用催化剂 |
在密闭容器中进行反应CH4(g)+H2O(g)  CO(g)+3H2(g)ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断不正确的是( )
CO(g)+3H2(g)ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断不正确的是( )
| A.10 min时,改变的外界条件可能是升高温度 |
| B.0~10 min内,v(H2)=0.15 mol·L-1·min-1 |
| C.恒温下,缩小容器体积,一段时间内v(逆)>v(正) |
| D.12 min时,反应达平衡的本质原因是气体总质量不再变化 |
在一定条件下的密闭容器中存在下列四个平衡体系,增大容器的体积对化学反应速率没有影响的是( )
A.2SO2+O2 2SO3 2SO3 |
B.CO+H2O(g) CO2+H2 CO2+H2 |
C.CO2(g)+H2O H2CO3 H2CO3 |
D.Fe3++3SCN- Fe(SCN)3 Fe(SCN)3 |
下列生产或实验事实引出的相应结论不正确的是( )
| | 事实 | 结论 |
| A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
| B | 工业制硫酸中,在SO3的吸收阶段,吸收塔里要装填瓷环 | 增大气液接触面积,使SO3的吸收速率增大 |
| C |  在容积可变的密闭容器中发生反应:2NH3(g)??N2H4(l)+H2(g),把容积的体积缩小一半 在容积可变的密闭容器中发生反应:2NH3(g)??N2H4(l)+H2(g),把容积的体积缩小一半 | 正反应速率加快,逆反应速率减慢 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得不同时间(t)内产生气体体积(V)的数据如图,根据图示分析实验条件,下列说法中一定不正确的是( )
| 组合 | 对应曲线 | c(HCl)/mol·L-1 | 反应温度/℃ | 铁的状态 |
| 1 | a | | 30 | 粉末状 |
| 2 | b | | 30 | 粉末状 |
| 3 | c | 2.5 | | 块状 |
| 4 | d | 2.5 | 30 | 块状 |
A.第1组实验中盐酸的浓度大于2.5 mol·L-1
B.第2组实验中盐酸的浓度等于2.5 mol·L-1
C.第3组实验的反应温度低于30 ℃
D.第4组实验的反应速率最慢
 2PbCrO4(s)+2H+(aq) ΔH<0
2PbCrO4(s)+2H+(aq) ΔH<0
