下列有关化学反应速率的说法不正确的是( )
| A.化学反应达到最大限度时,正逆反应速率也达到最大且相等 |
| B.催化剂能降低化学反应的活化能,加快反应速率,提高生产效率 |
| C.用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率 |
| D.用铁片和稀硫酸反应制H2比用98%的浓硫酸产生H2的速率快 |
石墨、金刚石燃烧的热化学方程式分别为:
C(石墨,s)+O2(g) CO2(g) ΔH="-393.51" kJ·mol-1
CO2(g) ΔH="-393.51" kJ·mol-1
C(金刚石,s)+O2(g) CO2(g) ΔH="-395.41" kJ·mol-1
CO2(g) ΔH="-395.41" kJ·mol-1
关于金刚石和石墨的相互转化,下列说法正确的是( )
| A.石墨转化成金刚石是自发进行的过程 |
| B.金刚石转化成石墨是自发进行的过程 |
| C.金刚石比石墨更稳定 |
| D.金刚石比石墨能量低 |
下列反应中,在高温下不能自发进行的是( )
A.CO(g) C(s)+O2(g) C(s)+O2(g) |
B.NH4Cl(s) NH3(g)↑+HCl(g)↑ NH3(g)↑+HCl(g)↑ |
C.(NH4)2CO3(s) NH4HCO3(s)+NH3(g) NH4HCO3(s)+NH3(g) |
D.MgCO3(s) MgO(s)+CO2(g) MgO(s)+CO2(g) |
在25 ℃、1.01×105 Pa下,反应2N2O5(g) 4NO2(g)+O2(g) ΔH="+56.7" kJ·mol-1能自发进行的合理解释是( )
4NO2(g)+O2(g) ΔH="+56.7" kJ·mol-1能自发进行的合理解释是( )
| A.该反应是分解反应 |
| B.该反应的熵增效应大于焓变效应 |
| C.该反应是熵减反应 |
| D.该反应是放热反应 |
对于化学反应能否自发进行,下列说法中错误的是( )
| A.若ΔH<0,ΔS>0,任何温度下都能自发进行 |
| B.若ΔH>0,ΔS<0,任何温度下都不能自发进行 |
| C.若ΔH>0,ΔS>0,低温时可自发进行 |
| D.若ΔH<0,ΔS<0,低温时可自发进行 |
下列事实不能用勒夏特列原理解释的是( )
①氯化铁溶液加热蒸干最终得不到氯化铁固体
②铁在潮湿的空气中容易生锈
③实验室可用排饱和食盐水的方法收集氯气
④常温下,将1 mL pH=3的醋酸加水稀释至100 mL,测得其pH<5
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)  K(g)+NaCl(l)
K(g)+NaCl(l)
⑥二氧化氮与四氧化二氮的平衡体系,加压后颜色加深
| A.①②③ | B.②⑥ | C.①③④⑤ | D.②⑤⑥ |
在密闭的容积可变的容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)  2C(g) ΔH<0。达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )
2C(g) ΔH<0。达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )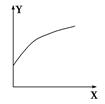
| | X | Y |
| A | 再加入A | B的转化率 |
| B | 降低温度 | 混合气体的密度 |
| C | 增大压强 | A的转化率 |
| D | 升高温度 | 混合气体的平均摩尔质量 |
在某恒容的密闭容器中,可逆反应A(g)+B(g)  xC(g)有如图所示的关系曲线,下列说法正确的是( )
xC(g)有如图所示的关系曲线,下列说法正确的是( )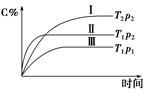
| A.温度:T1>T2 | B.压强:p1>p2 |
| C.正反应是吸热反应 | D.x的值是2 |
在容积一定的密闭容器中,反应A(?)+B(g)  C(g)+D(g)达到平衡后,升高温度容器
C(g)+D(g)达到平衡后,升高温度容器
内气体的密度增大,则下列叙述正确的是( )
| A.正反应是放热反应 |
| B.A不是气态物质,加入A该平衡向正反应方向移动 |
| C.其他条件不变,加入A平衡不移动 |
| D.改变压强对该平衡的移动无影响 |
已知CO和H2在一定条件下合成甲醇的反应为CO(g)+2H2(g)  CH3OH(g)。现在容积均为1 L的a、b、c三个密闭容器中分别充入1 mol CO和2 mol H2的混合气体,控制温度进行反应,测得相关数据的关系如图所示。下列说法正确的是( )
CH3OH(g)。现在容积均为1 L的a、b、c三个密闭容器中分别充入1 mol CO和2 mol H2的混合气体,控制温度进行反应,测得相关数据的关系如图所示。下列说法正确的是( )
| A.正反应的ΔH>0 |
| B.反应进行到5 min时,b容器中v正=v逆 |
| C.减压可将b中的平衡状态转变成c中的平衡状态 |
| D.达到平衡时,a、b、c中CO的转化率为b>a>c |