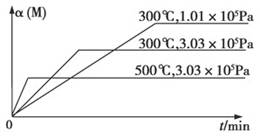
已知(CH3COOH)2(g)  2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量
2CH3COOH(g),经实验测得不同压强下,体系的平均摩尔质量 随温度(T)的变化曲线如图所示,下列说法正确的是( )
随温度(T)的变化曲线如图所示,下列说法正确的是( )
| A.该过程的ΔH<0 |
| B.气体压强:p(a)<p(b)=p(c) |
| C.平衡常数:K(a)=K(b)<K(c) |
| D.测定乙酸的相对分子质量要在高压、低温条件 |
NO2和N2O4可相互转化:2NO2(g)  N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是
N2O4(g) ΔH<0现将一定量NO2和N2O4的混合气体通入体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图。下列说法中正确的是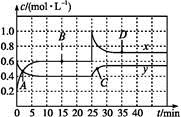
| A.图中共有两条曲线x和y,其中曲线y表示NO2浓度随时间的变化 |
| B.A、B、C、D四个点中,表示化学反应处于平衡状态的点是B和C |
| C.反应进行至25 min时,曲线发生变化的原因是加入0.4 mol N2O4 |
| D.若要达到与D相同的状态,在25 min时还可采取的措施是适当缩小容器体积 |
一定条件下,在密闭容器中,能表示反应X(g)+2Y(g)  2Z(g)一定达到化学平衡状态的是
2Z(g)一定达到化学平衡状态的是
①X、Y、Z的物质的量之比为1∶2∶2 ②X、Y、Z的浓度不再发生变化 ③容器中的压强不再发生变化 ④单位时间内生成n mol Z,同时生成2n mol Y
| A.①② | B.①④ | C.②③ | D.③④ |
将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是
| A.2v(NH3)=v(CO2) |
| B.密闭容器中c(NH3)∶c(CO2)=2∶1 |
| C.密闭容器中混合气体的密度不变 |
| D.密闭容器中氨气的体积分数不变 |
设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) ΔH=a kJ/mol,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH=a kJ/mol,反应②Fe(s)+H2O(g)  FeO(s)+H2(g) ΔH=b kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH=b kJ/mol,以上两反应的平衡常数分别为K1和K2。在不同温度下,K1、K2的值如下:
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
下列有关叙述正确的是( )
A.b<0
B.在973 K下增大压强,K2增大
C.a>b
D.在常温下反应①一定能自发进行
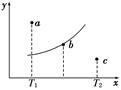
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)  SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是( )
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是( )
| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
| D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 |
一定条件下的密闭容器中:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是( )
4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是( )
| A.4 mol NH3和5 mol O2反应,达到平衡时放出的热量为905.9 kJ |
B.平衡时v正(O2)=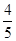 v逆(NO) v逆(NO) |
| C.平衡后降低压强,混合气体平均摩尔质量增大 |
| D.平衡后升高温度,混合气体中NO含量降低 |
下列说法正确的是( )
| A.一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)的ΔH>0 ΔS>0 |
| B.凡是放热反应都是自发的,凡是吸热反应都是非自发的 |
C.常温下,2H2O 2H2↑+O2↑,即常温下水的分解反应是自发反应 2H2↑+O2↑,即常温下水的分解反应是自发反应 |
| D.对于反应H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
 3C(g)+D(s) ΔH1>0,②xM(g)+N(g)
3C(g)+D(s) ΔH1>0,②xM(g)+N(g) 3Q(g) ΔH2。反应①中各物质与反应②中各物质均不发生反应。在某容器里只进行反应②,M的转化率与温度、压强的关系如图所示。
3Q(g) ΔH2。反应①中各物质与反应②中各物质均不发生反应。在某容器里只进行反应②,M的转化率与温度、压强的关系如图所示。