某反应能量变化如右下图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列叙述正确的是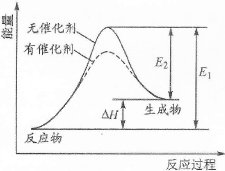
| A.该反应为放热反应 |
| B.催化剂能改变反应的焓变 |
| C.催化剂能降低反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |
未来新能源的特点是资源丰富,使用时污染很小,可再生。下列符合未来新能源标准的是:①天然气 ②煤 ③石油 ④太阳能 ⑤生物质能 ⑥风能 ⑦氢能
| A.①②③④ | B.④⑤⑥⑦ | C.③⑤⑥⑦ | D.③④⑤⑥⑦ |
已知:①CO(g)+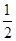 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②H2(g)+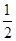 O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8 kJ·mol-1
则CO(g)+H2O(g)=H2(g)+CO2(g)的ΔH为
| A.+41.2 kJ?mol-1 | B.-41.2 kJ?mol-1 | C.+82.4kJ?mol-1 | D.-524.8 kJ?mol-1 |
下列说法正确的是
| A.CO能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应 |
| B.1 mol硫酸与1 mol Ba(OH)2完全中和所放出的热量为中和热 |
| C.相同条件下,2mol氢原子所具有的能量大于1mol氢分子所具有的能量 |
| D.101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 |
下列反应中生成物的总能量大于反应物总能量的非氧化还原反应是
| A.铝热反应 | B.氯化铝溶液的水解 |
| C.氢氧化钠和盐酸反应 | D.焦炭在高温下与水蒸气反应 |
含20.0 g NaOH的稀溶液与稀盐酸完全反应时,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是
A.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" +28.7" kJ·mol-1 =" +28.7" kJ·mol-1 |
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" -28.7" kJ·mol-1 =" -28.7" kJ·mol-1 |
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" +57.4" kJ·mol-1 =" +57.4" kJ·mol-1 |
D.NaOH(aq)+HCl(aq)=NaCl(aq)+H20(l) =" -57.4" kJ·mol-1 =" -57.4" kJ·mol-1 |
下列反应中,生成物的总能量大于反应物的总能量的是
| A.氢气在空气中燃烧 | B.氢氧化钡晶体与氯化铵晶体反应 |
| C.盐酸与氨氧化钠溶液反应 | D.锌与稀硫酸反应制取氢气 |
下列反应中的能量变化关系符合下图所示的是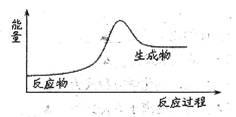
| A.盐酸与烧碱反应 | B.天然气燃烧 |
| C.三氧化硫与水反应 | D.煅烧石灰石 |
已知反应:
①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
下列结论正确的是( )
| A.碳的燃烧热等于110.5 kJ·mol-1 |
| B.2mol C(s)在1 mol O2(g)燃烧,放出221 kJ热量 |
| C.1L0.1 mol/L H2SO4溶液与1L0.1 mol/L NaOH溶液反应,放出5.73 kJ热量 |
| D.pH=3的醋酸与pH=11的NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
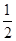 O2(g) ===CO(g);ΔH1 C(s)+O2(g) ===CO2(g);ΔH2
O2(g) ===CO(g);ΔH1 C(s)+O2(g) ===CO2(g);ΔH2