题目内容
某反应能量变化如右下图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列叙述正确的是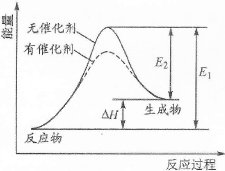
| A.该反应为放热反应 |
| B.催化剂能改变反应的焓变 |
| C.催化剂能降低反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |
C
解析试题分析:A、总能量:反应物<生成物,则该反应是吸热反应,错误;B、催化剂只能降低反应的活化能,不能改变反应的焓变,错误;D、读图可知活化能:正反应>逆反应,错误。
考点:考查化学反应过程中的能量变化示意图等相关知识。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可以用盖斯定律间接求得。已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出x kJ热量;已知每摩尔单质碳完全燃烧生成CO2放出热量为y kJ,则1 mol C与O2反应生成CO的反应热ΔH为
| A.-y kJ·mol-1 | B.-(10x-y)kJ·mol-1 |
| C.-(5x-0.5y)kJ·mol-1 | D.+(10x-y)kJ·mol-1 |
已知在1×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是
A.H2O(g)=H2(g)+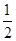 O2(g)ΔH=242 kJ·mol-1 O2(g)ΔH=242 kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l)ΔH=-484 kJ·mol-1 |
C.H2(g)+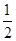 O2(g)=H2O(g)ΔH=242 kJ·mol-1 O2(g)=H2O(g)ΔH=242 kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g)ΔH=484 kJ·mol-1 |
下列反应中生成物的总能量大于反应物总能量的非氧化还原反应是
| A.铝热反应 | B.氯化铝溶液的水解 |
| C.氢氧化钠和盐酸反应 | D.焦炭在高温下与水蒸气反应 |
与图像有关的叙述,正确的是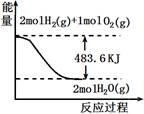
| A.表示1mol H2 (g)完全燃烧生成水蒸气吸收241.8 kJ热量 |
| B.表示的热化学方程式为:H2(g)+ 1/2 O2(g) → H2O(g) +241.8 kJ |
| C.表示2 mol H2(g)所具有的能量一定比2 mol气态水所具有的能量多483.6 kJ |
| D.H2O(g)的能量低于H2(g)和O2(g)的能量之和 |
肼(N2H4)是一种可用于火箭或原电池的燃料。已知:
N2(g) + 2O2(g) =2 NO2(g) ΔH =" +67.7kJ/mol" ①
N2H4(g) + O2(g) = N2(g) + 2H2O(g) ΔH = -534 kJ/mol ②
下列说法正确的是
| A.反应①中反应物所具有的总能量大于生成物所具有的总能量 |
| B.2N2H4(g) + 2NO2(g) = 3N2(g)+ 4H2O (g) ΔH = -1000.3kJ/mol |
| C.铂做电极,KOH溶液做电解质溶液,由反应②设计的燃料电池其负极反应式:N2H4-4e-+4OH-=N2+4H2O |
| D.铂做电极,KOH溶液做电解质溶液,由反应②设计的燃料,工作一段时间后,KOH溶液的pH将增大 |
如下图所示,△H1=-393.5 kJ?mol-1,△H2=-395.4 kJ?mol-1,下列说法或表示式正确的是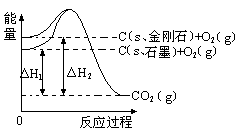
| A.石墨和金刚石的转化是物理变化 |
| B.1mol石墨的总能量比1 mol金刚石的总能量大1.9 kJ |
| C.金刚石的稳定性强于石墨 |
| D.C(s、石墨)=C(s、金刚石) △H=" +1.9" kJ?mol-1 |
关于中和热测定实验的下列说法不正确的是
| A.烧杯间填满碎泡沫塑料是为了减少实验过程中的热量损失 |
| B.使用环形玻璃棒既可以搅拌又避免损坏温度计 |
| C.向盛装酸的烧杯中加碱时要小心缓慢 |
| D.测了酸后的温度计要用水清洗后再测碱的温度 |
在298 K、100 kPa时,已知:
2H2O(g)=O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)=2HCl(g) ΔH2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是 ( )。
| A.ΔH3=ΔH1+2ΔH2 | B.ΔH3=ΔH1+ΔH2 |
| C.ΔH3=ΔH1-2ΔH2 | D.ΔH3=ΔH1-ΔH2 |