下列说法中不正确的是
| A.开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 |
| B.钢铁是用量最大、用途最广泛的合金 |
| C.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| D.利用催化设施,可以将汽车尾气中CO和NO转化为无害气体 |
已知: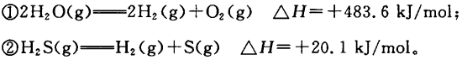
下列判断正确的是 ( )
| A.氢气的燃烧热:△H="-241.8" kJ/mol |
| B.相同条件下,充分燃烧1 mol H2(g)与1 molS(g)的混合物比充分燃烧1 molH2S (g)放热多20.1 kJ |
| C.由①②知,水的热稳定性小于硫化氢 |
| D.②中若生成固态硫,△H将增大 |
下列图示与对应的叙述相符的是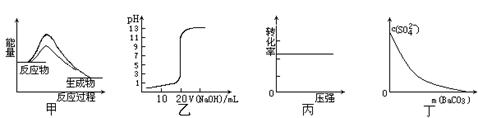
| A.图甲表示使用催化剂后,该反应的ΔH变小 |
| B.图乙表示0.10mol·L-1 NaOH溶液滴定20.00mL0.10mol·L-1 CH3COOH溶液所得到的 滴定曲线 |
C.图丙表示反应H2(g) + I2(g)  2HI(g)中H2的转化率随压强的变化 2HI(g)中H2的转化率随压强的变化 |
| D.图丁表示在饱和Na2SO4溶液中逐步加BaCO3固体后,溶液中c(SO42-)的浓度变化 |
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如下图为N2(g)与 O2(g)反应生成NO(g)过程中的能量变化:
下列说法正确的是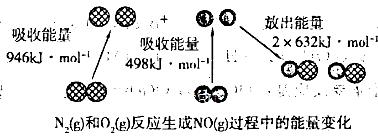
| A.1 mol N2(g)和1 molO2 (g)具有的总能量大于 2 mol NO(g)具有的总能量 |
| B.1 molN2 (g)和l molO2 (g)反应生成2 mol NO(g)吸收180 kJ热量. |
| C.通常情况下N2(g)和O2(g)混合能直接反应生成NO |
| D.数据不足,不能确定反应热的大小 |
下列与化学反应能量变化相关的叙述正确的是
A.同温同压下, 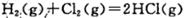 在光照和点燃条件的△H不同。 在光照和点燃条件的△H不同。 |
| B.相同条件下2mol氢原子所具有的能量小于1 mol氢分子所具有的能量 |
| C.应用盖斯定律,可以计算某些难以直接测量的反应焓变 |
D.反应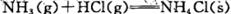 在室温下可自发进行:则该反应的△H>0 在室温下可自发进行:则该反应的△H>0 |
下列关于反应热的说法正确的是
| A.当△H<O时,表示该反应为吸热反应 |
B.已知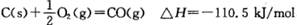 ,说明碳的燃烧热为110kJ/mol ,说明碳的燃烧热为110kJ/mol |
| C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
| D.化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
下列设备工作时,将化学能转化为热能的是( )。
| A | B | C | D |
 |  |  |  |
| 硅太阳能电池 | 锂离子电池 | 太阳能集热器 | 燃气灶 |
已知1 mol红磷转化为1 mol白磷,吸收18.39 kJ热量。
①4P(红,s)+5O2(g)=2P2O5(s);ΔH1
②P4(白,s)+5O2(g)=2P2O5(s);ΔH2
则ΔH1与ΔH2的关系正确的是( )
| A.ΔH1=ΔH2 | B.ΔH1>ΔH2 |
| C.ΔH1<ΔH2 | D.无法确定 |
反应A(g)+B(g)→C(g) ΔH分两步进行:①A(g)+B(g)→X(g)ΔH1 ②X(g)→C(g) ΔH2,反应过程中能量变化如图所示,E1表示A(g)+B(g)→X(g)的活化能,下列说法正确的是( )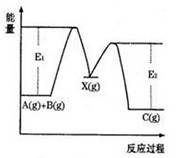
| A.ΔH1=ΔH-ΔH2>0 |
| B.X是反应A(g)+B(g)→C(g)的催化剂 |
| C.E2是反应②的活化能 |
| D.ΔH=E1-E2 |
发射用的运载火箭使用的是以液氢为燃烧剂,液氧为氧化剂的高能低温推进剂。
已知:H2(g)+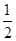 O2(g)=H2O(l)
O2(g)=H2O(l)
ΔH1=-285.8 kJ·mol-1①
H2(g)=H2(l) ΔH2=-0.92 kJ·mol-1②
O2(g)=O2(l) ΔH3=-6.84 kJ·mol-1③
H2O(g)=H2O(l) ΔH4=-44 kJ·mol-1④
下列说法正确的是( )
| A.上述四个反应都是吸热反应 |
| B.1 mol液态H2的能量大于1 mol气态H2的能量 |
| C.H2的燃烧热ΔH为-285.8 kJ·mol-1 |
D.火箭中液氢燃烧的热化学方程式为H2(l)+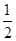 O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1 O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1 |