已知甲烷燃烧生成二氧化碳和液态水放出的热量为55.625 kJ·g-1。下列热化学方程式中不正确的是( )
A.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH ="-890" kJ/mol CO2(g)+2H2O(l) ΔH ="-890" kJ/mol |
B.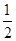 CH4(g)+O2(g) CH4(g)+O2(g) 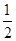 CO2(g)+H2O(l) ΔH="-445" kJ/mol CO2(g)+H2O(l) ΔH="-445" kJ/mol |
C.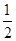 CO2(g)+H2O(l) CO2(g)+H2O(l) 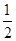 CH4(g)+O2(g) ΔH="+445" kJ/mol CH4(g)+O2(g) ΔH="+445" kJ/mol |
D.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH="-55.625" kJ/mol CO2(g)+2H2O(l) ΔH="-55.625" kJ/mol |
红磷(P)和Cl2发生反应生成PCl3和PCl5,反应过程和能量的关系如下图所示,图中的ΔH表示生成1 mol产物的数据。已知PCl5分解生成PCl3和Cl2,该分解反应是可逆反应。下列说法正确的是( )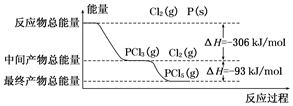
| A.其他条件不变,升高温度有利于PCl5的生成 |
| B.反应2P(s)+5Cl2(g)=2PCl5(g)对应的反应热 ΔH=-798 kJ/mol |
| C.P和Cl2反应生成PCl3的热化学方程式为:2P(s)+3Cl2(g)=2PCl3(g) ΔH=-306 kJ/mol |
| D.其他条件不变,对于2PCl5(g)=2P(s)+5Cl2(g) ΔH反应,增大压强,PCl5的转化率减小,ΔH减小 |
已知:① 2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1 ②H2(g)+S(g)=H2S(g) ΔH=-20.1 kJ·mol-1。
下列判断正确的是( )
| A.1 mol氢气完全燃烧生成液态水吸收热量241.8 kJ |
| B.1 mol H2O(g)和1 mol H2S(g)的能量相差221.7 kJ |
| C.由①②知,水的热稳定性小于硫化氢 |
| D.若反应②中改用固态硫,1 mol S(s)完全反应,放出的热量小于20.1 kJ |
下列设备工作时,将化学能转化为热能的是( )
| A | B | C | D |
 |  |  |  |
| 硅太阳能电池 | 锂离子电池 | 太阳能集热器 | 燃气灶 |
下列说法或表示方法不正确的是( )
| A.盖斯定律实质上是能量守恒定律的体现 |
| B.在稀溶液中:H+(aq)+OH-(aq)=H2O(l);ΔH= -57.3 kJ/mol,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
| C.由C(石墨)―→C(金刚石);ΔH=+73 kJ/mol,可知石墨比金刚石稳定 |
| D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);ΔH=-285.8 kJ/mol |
下列说法不正确的是( )
| A.反应是放热还是吸热必须看生成物和反应物所具有的总能量的相对大小 |
| B.绿色植物进行光合作用时,将太阳能转化为化学能储存起来 |
| C.吸热反应中由于反应物总能量小于生成物总能量,因而无利用价值 |
| D.物质的化学能可以在一定条件下转化为热能、电能为人类所利用 |
下列各组热化学方程式中,Q1<Q2的是( )
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-Q1 kJ·mol-1 CH4(g)+3/2O2(g)=CO(g)+2H2O(g) ΔH=-Q2 kJ·mol-1 |
| B.S(g)+O2(g)=SO2(g) ΔH=-Q1 kJ·mol-1 S(s)+O2(g)=SO2(g) ΔH=-Q2 kJ·mol-1 |
| C.H2(g)+Br2(g)=2HBr(g) ΔH=-Q1 kJ·mol-1 H2(g)+Cl2(g)=2HCl(g) ΔH=-Q2 kJ·mol-1 |
| D.HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) ΔH=-Q1 kJ·mol-1 |
某一化学反应在不同条件下的能量变化曲线如下图所示。下列说法正确的是( )
| A.化学催化比酶催化的效果好 |
| B.使用不同催化剂可以改变反应的热效应 |
| C.使用不同催化剂可以改变反应的能耗 |
| D.反应物的总能量低于生成物的总能量 |
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:
mCeO2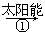 (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xH2O+xCO2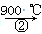 mCeO2+xH2+xCO
mCeO2+xH2+xCO
下列说法不正确的是( )
A.该过程中CeO2没有消耗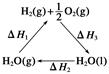 |
| B.该过程实现了太阳能向化学能的转化 |
| C.图中ΔH1=ΔH2+ΔH3 |
| D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH--2e-=CO32-+2H2O |
能源是当今社会发展的三大支柱之一。有专家提出:如果能够利用太阳能使燃料燃烧产物(如CO2、H2O、N2等)重新组合(如下图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为( )
| A.化学能 | B.热能 | C.生物能 | D.电能 |