下列反应一定属于放热反应的是( )。
| A.氢氧化钡晶体和氯化铵晶体的反应 |
B.能量变化如图所示的反应 |
| C.化学键断裂吸收的能量比化学键形成放出的能量少的反应 |
| D.不需要加热就能发生的反应 |
25℃、101kPa下,碳、氢气和甲烷的燃烧热依次是393.5 kJ·mol—1、285.8 kJ·mol—1
和890.3kJ·mol—1,下列选项中正确的是
| A.2H2(g)+O2(g)=2H2O(l)△H=—285.8kJ·mol—1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890.3kJ·mol—1 |
| C.H2(g)+1/2O2(g)=H2O(g)△H<—285.8kJ·mol—1 |
| D.C(s)+2H2(g)=CH4(g)△H=—74.8 kJ·mol—1 |
根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( )
| A.H2O分解为H2与O2时放出热量 |
| B.生成1mol H2O时吸收热量245kJ |
| C.甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙 |
| D.氢气和氧气的总能量小于水的能量 |
北京奥运会开幕式在李宁点燃鸟巢主火炬时达到高潮。奥运火炬采用的是环保型燃料——丙烷,其燃烧时发生反应的化学方程式为C3H8+5O2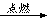 3CO2+4H2O。下列说法中不正确的是( )
3CO2+4H2O。下列说法中不正确的是( )
| A.火炬燃烧时化学能只转化为热能 |
| B.所有的燃烧反应都会释放热量 |
| C.1mol C3H8和5mol O2所具有的总能量大于3mol CO2和4mol H2O所具有的总能量 |
| D.丙烷完全燃烧的产物对环境无污染,故丙烷为环保型燃料 |
下列说法中正确的是( )
| A.物质发生化学反应时都伴随着能量变化,伴随能量变化的物质变化一定是化学变化 |
| B.需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应 |
| C.吸热反应就是反应物的总能量比生成物的总能量高;也可以理解为化学键断裂时吸收的能量比化学键形成时放出的能量多 |
| D.因为3O2=2O3是吸热反应,所以臭氧比氧气的化学性质更活泼 |
节能减排与我们的生活息息相关,参与节能减排是每一位公民应尽的义务。下列举措不符合这一要求的是( )
| A.为推广氢能的使用,工业上可采用电解水法制取大量氢气 |
| B.将石油裂化、裂解,综合利用石油资源 |
| C.有节制地开采煤、石油、天然气等矿物资源 |
| D.将某些废旧塑料熔化后再成型 |
近年来,全球气候变暖给人类的生存和发展带来了严峻的挑战,在此背景下,“新能源”、“低碳”、“节能减排”、“吃干榨尽”等概念愈来愈受到人们的重视。下列有关说法不正确的是( )
| A.太阳能、地热能、生物质能和核聚变能均属于“新能源” |
| B.“低碳”是指采用含碳量低的烃类作为燃料 |
C.下图甲烷经一氯甲烷生成低碳烯烃的途径体现了“节能减排”思想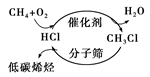 |
| D.让煤变成合成气,把煤“吃干榨尽”,实现了煤的清洁、高效利用 |
下列过程有热量放出的是
| A.断开氢气中的H-H键 |
| B.C与H2O(g)反应 |
| C.Ba(OH)2·8H2O晶体与NH4Cl晶体反应 |
| D.Na与H2O反应 |
下列依据热化学方程式得出的结论正确的是( )
| A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ· mol—1则氢气的燃烧热为△H=-241.8 kJ· mol—1 |
| B.已知C(石墨,s)=C(金刚石,s);△H=+1.9kJ·mol-1,可知石墨比金刚石更稳定 |
| C.已知NaOH(ag)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4 kJ· mol—1可知:含1mol CH3COOH的溶液与含1mol NaOH的溶液混合,放出热量等于57.4 kJ |
| D.已知2C(s)+2O2(g)=2CO2(g);△H1 2C(s)+O2(g)=2CO(g);△H2,则△H1>△H2 |
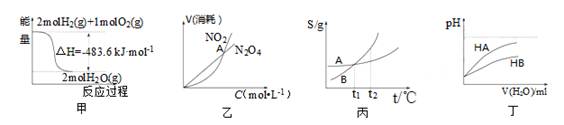
 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态