已知1 g氢气完全燃烧生成液态水时放出热量143 kJ,18 g水蒸气变成液态水放出44kJ的热量。其它相关数据如下表,则表中X为:
| | O=O(g) | H-H(g) | H-O(g) |
| 1mol化学键断裂时需要吸收的能量/kJ | 496 | X | 463 |
某一化学反应在不同条件下的能量变化曲线如右图所示。下列说法正确的是
| A.化学催化比酶催化的效果好 |
| B.使用不同催化剂可以改变反应的热效应 |
| C.使用不同催化剂可以改变反应的能耗 |
| D.反应物的总能量低于生成物的总能量 |
下列说法正确的是
已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
| A.H2(g)的燃烧热为571.6 kJ·mol-1 |
| B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
| C.H2SO4(aq)+Ba(OH)2(aq)==BaSO4(s)+H2O(l)ΔH=-57.3 kJ·mol-1 |
| D.3H2(g)+CO2(g)=CH3OH(l)+H2O(l)ΔH=+135.9 kJ·mol-1 |
已知下列热化学方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol
Fe2O3(s)+CO(g)= Fe3O4(s)+CO2(g) ΔH=-15.73 kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+640.4 kJ/mol
则14 g CO气体还原足量FeO固体得到Fe单质和CO2气体时对应的ΔH约为
| A.-218 kJ/mol | B.-109 kJ/mol | C.+218 kJ/mol | D.+109 kJ/mol |
已知298K时,2SO2(g)+O2(g) 2SO3(g);△H=-197kJ·mol-1。现有同一温度下的三个体积相同的密闭容器,在第一个容器中通入2molSO2和1molO2,达到平衡时,反应放出的热量为Q1;向第二个密闭容器中通入1molSO2和0.5molO2,达到平衡时放出的热量为Q2;在第三个密闭容器中通入1molSO2、0.5molO2和1molSO3达到平衡时放出的热量为Q3。下列关系正确的是
2SO3(g);△H=-197kJ·mol-1。现有同一温度下的三个体积相同的密闭容器,在第一个容器中通入2molSO2和1molO2,达到平衡时,反应放出的热量为Q1;向第二个密闭容器中通入1molSO2和0.5molO2,达到平衡时放出的热量为Q2;在第三个密闭容器中通入1molSO2、0.5molO2和1molSO3达到平衡时放出的热量为Q3。下列关系正确的是
| A.Q1=Q3=197kJ | B.Q1=Q3<197kJ |
| C.Q1=2Q2 <197kJ | D.Q2<Q1<197kJ |
用Cl2生产某些含氯有机物时会产生副产物HCl。 利用反应A:4HCl+O2 2Cl2+2H2O,
2Cl2+2H2O,
可实现氯的循环利用。
已知:Ⅰ.反应A中,4mol HCl被氧化,放出115.6kJ的热量.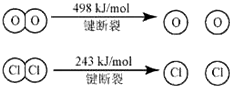
Ⅱ.则断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为
| A.16kJ | B.24kJ | C.32kJ | D.48kJ |
下列变化属于吸热反应的是
①碳与二氧化碳化合
②生石灰与水反应生成熟石灰
③Zn与稀硫酸反应
④氯酸钾分解制氧气
⑤Ba(OH)2.8H2O与NH4Cl反应
⑥甲烷与氧气的燃烧
| A.①④ | B.②③ | C.①④⑤ | D.①②④ |
用浓氯化铵溶液处理过的舞台幕布不易着火。其原因是
①幕布的着火点升高
②幕布的质量增加
③氯化铵分解吸收热量,降低了温度
④氯化铵分解产生的气体隔绝了空气
| A.①② | B.①③ | C.②④ | D.③④ |
下列不属于生物质能的利用的是
| A.燃烧树枝取热 | B.将植物秸杆制沼气 |
| C.用淀粉制乙醇 | D.用太阳能发电 |