已知H—H键能为436 kJ·mol-1,N—H键能为391 kJ·mol-1,根据化学方程式:N2(g)+3H2(g) 2NH3(g) ΔH="-92.4" kJ·mol-1,则N≡N键的键能是( )
2NH3(g) ΔH="-92.4" kJ·mol-1,则N≡N键的键能是( )
| A.431 kJ·mol-1 | B.946 kJ·mol-1 |
| C.649 kJ·mol-1 | D.896 kJ·mol-1 |
下列说法中正确的是
| A.生成物总能量一定低于反应物总能量 |
B.同温同压下,H2(g)+Cl2(g)=2HCl(g) 在光照和点燃条件下的 H不同 H不同 |
C.一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3气,放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) 2NH3(g)  H =-38.6 kJ/mol H =-38.6 kJ/mol |
| D.一定条件下4 HCl(g)+O2(g)=2Cl2(g)+2H2O(g) ,当1 mol |
H-O键与断裂1 mol H-Cl键所需能量差为31.9 kJ

关于下图所示转化关系(X代表卤素),说法不正确的是
| A.2H(g) +2X(g) ="=" 2HX(g) ΔH3<0 |
| B.途径Ⅰ生成HX的反应热与途径无关,所以ΔH1 = ΔH2 + ΔH3 |
| C.Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多 |
| D.途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定 |
下列说法不正确的是
A.已知H2(g)+ O2(g)===H2O(g) ΔH1=a kJ·mol-1; O2(g)===H2O(g) ΔH1=a kJ·mol-1;2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1,则a>b |
| B.CO的燃烧热为283.0 kJ·mol-1,则 2CO2(g)===2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1 |
C.若N2(g)+3H2(g)  2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ 2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ |
| D.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和KOH反应的中和热ΔH=-114.6 kJ·mol-1 |
某反应的反应过程中能量变化如图1 所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
| A.该反应为放热反应 |
| B.催化剂能改变该反应的焓变 |
| C.催化剂能降低该反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |
下列图示与对应的叙述相符的是 
| A.图Ⅰ中 可以看出反应A(g)=C(g)的△H=(E1-E4)kJ·mol-1 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是扩大了容器的体积 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是扩大了容器的体积 |
| C.图Ⅲ表示将CO2通入NaOH的稀溶液中,随着CO2的通入,溶液中水电离出的c(H+)变化关系 |
| D.图Ⅳ曲线表示用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由此可判断HX的酸性最强 |
下列说法中正确的是( )
| A.伴有能量变化的物质变化都是化学变化 | B.物质发生化学反应一定伴随着能量变化 |
| C.吸热反应在常温下不能发生 | D.放热反应的发生无需任何条件 |
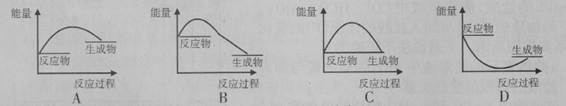
下列反应前后物质的总能量变化能用下图表示的是( )
| A.生石灰和水的反应 |
| B.石灰石在高温下的分解反应 |
| C.盐酸与氢氧化钠溶液的反应 |
| D.木炭在氧气中燃烧 |
下列有关能量的说法不正确的是 ( )
| A.化石能源物质内部贮存着大量的能量 |
| B.植物的光合作用使太阳能转化为化学能 |
| C.燃料燃烧时只是将化学能转化为热能 |
| D.由石墨制金刚石是吸热反应,故石墨能量比金刚石能量低 |