下列说法正确的是
| A.镀锌铁和镀锡铁的镀层破损后,前者较易被腐蚀 |
| B.火电是将燃料中的化学能直接转化为电能的过程 |
| C.将煤粉碎了再燃烧可以提高煤的燃烧效率 |
| D.化学反应的限度不可以通过改变条件而改变 |
据人民网报道,有一集团拟在太空建立巨大的激光装置,把太阳光变成激光用于分解海水制氢气,其反应式可表示为:2H2O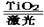 2H2↑+O2↑。有下列几种说法:①水的分解反应是放热反应;②氢气是一级能源;③使用氢气作燃料有助于控制温室效应;④该过程将光能转化为化学能,以上叙述中正确的是
2H2↑+O2↑。有下列几种说法:①水的分解反应是放热反应;②氢气是一级能源;③使用氢气作燃料有助于控制温室效应;④该过程将光能转化为化学能,以上叙述中正确的是
| A.①② | B.②③ | C.③④ | D.①②③④ |
在人类生产、生活所需能量日益增多的今天,研究化学反应及其能量变化对合理利用常规能源和开发新能源具有十分重要的意义。下列说法中不正确的是
| A.任何化学反应都伴随着能量的变化 |
| B.化学反应中的能量变化都表现为热量的变化 |
| C.反应物的总能量高于生成物的总能量,反应释放能量 |
| D.若化学键形成时释放的能量小于旧化学键被破坏时需要吸收的能量,反应吸收能量 |
下列设备工作时,将化学能转化为热能的是
| A | B | C | D |
 |  |  |  |
| 硅太阳能电池 | 锂离子电池 | 太阳能集热器 | 燃气灶 |
已知:25℃,101KPa下,固体白磷、固体红磷分别充分燃烧,放出热量如下:
①P(s,白磷)+5/4 O2(g)=" 1/4" P4O10(s) 放出755.2kJ的热
②P(s,红磷)+5/4 O2(g)=" 1/4" P4O10(s) 放出738.5kJ的热
据此判断下列说法中正确的是
| A.由白磷变红磷是吸热反应 |
| B.白磷、红磷都是磷的单质,相互可以自由转化,不吸热,也不放热 |
| C.等质量时,白磷比红磷具有的能量高 |
| D.等物质的量时,断白磷分子中的键比断红磷分子中的键消耗的能量多 |
已知:断开1molN≡N需要吸收akJ热量,断开1molH—H需要吸收bkJ热量,断开1molN—H需要吸收ckJ热量。向某密闭容器中通入1molN2和3molH2,在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g)(放热反应)。下列描述中正确的是
2NH3(g)(放热反应)。下列描述中正确的是
| A.N2和H2具有的总能量一定比NH3具有的总能量低 |
| B.a、b、c三者的关系为:a+3b<2c |
| C.向密闭容器中通入1molN2和3molH2,反应放出的热量必为(6c―a―3b)kJ |
| D.形成1molN—H会放出ckJ热量 |
白磷会对人体造成严重的烧伤,白磷(P4)分子结构为 。下列说法不正确的是
。下列说法不正确的是
| A.白磷着火点低,在空气中可自燃 |
| B.白磷、红磷互为同素异形体 |
| C.31 g白磷中,含P—P键1.5 mol |
| D.已知P4(白磷,s)+3O2(g)===2P2O3(s) ΔH=-Q kJ·mol-1,则白磷的燃烧热为Q kJ·mol-1 |
已知:
2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
Na2O2(s)+CO2(g)===Na2CO3(s)+ O2(g) ΔH=-266 kJ·mol-1
O2(g) ΔH=-266 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
| A.CO的燃烧热为283 kJ |
| B.下图可表示由CO生成CO2的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>-532kJ·mol-1 |
| D.CO(g)与Na2O2(s)反应放出549 kJ热量时,电子转移数为6.02×1023 |

下列变化为放热的化学反应的是 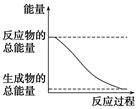
| A.H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1 |
| B.2HI(g)===H2(g)+I2(g) ΔH=+14.9 kJ·mol-1 |
| C.形成化学键时共放出862 kJ能量的化学反应 |
| D.能量变化如右图所示的化学反应 |
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
已知:
①Sn(白,s)+2HCl(aq)===SnCl2(aq)+H2(g) ΔH1
②Sn(灰,s)+2HCl(aq)===SnCl2(aq)+H2(g) ΔH2
③Sn(灰,s)  Sn(白,s)ΔH3=+2.1 kJ·mol-1
Sn(白,s)ΔH3=+2.1 kJ·mol-1
下列说法正确的是
| A.ΔH1>ΔH2 |
| B.锡在常温下以灰锡状态存在 |
| C.灰锡转化为白锡的反应是放热反应 |
| D.锡制器皿长期处在低于13.2 ℃的环境中,会自行毁坏 |