已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是 ( )
已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是 ( )
| A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=-2b kJ ? mol-1 |
| B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l);ΔH=2b kJ ? mol-1 |
| C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=-4b kJ ? mol-1 |
| D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=b kJ ? mol-1 |
已知反应: ①2C(s)+O2(g)=2CO(g)△H=-221kJ/mol
②H+(aq)+OH-(aq)=H2O(1);△H=-57.3kJ/mol 下列结论正确的是( )
| A.碳的燃烧热大于110.5kJ/mol |
| B.反应①放出的热量为221kJ |
| C.稀硫酸与稀氨水溶液反应的中和热为-57.3kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
有关下列各组热化学方程式中关系说法正确的是
2H2(g)+O2(g)=2H2O(g); △H1= -Q1kJ/mol
2H2(g)+O2(g)=2H2O(1); △H2= -Q2kJ/mol
H2(g)+1/2O2(g)=H2O(1);△H3= -Q3kJ/mol
| A.△H1=△H2 | B.△H1<△H2 | C.Q1 >2Q3 | D.△H1>2△H3 |
下列叙述正确的是
A.在0.10 mol·L-1 NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)+c(CO ) ) |
| B.甲烷的标准燃烧热是890.3 kJ·mol-1,则甲烷燃烧的热化学方程式是: CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3 kJ·mol-1 |
| C.用铜作电极电解CuSO4溶液:2Cu2++2H2O 电解 2Cu+O2↑+4H+ |
| D.以KOH为电解质溶液的甲醇燃料电池的负极电极反应式: |
下列依据相关数据作出的推理和判断中,不正确的是
| A.依据相对分子质量的数据,推测乙醇和丙烷沸点的相对高低 |
| B.依据溶解度的数据,选择用重结晶的方法可将粗苯甲酸提纯 |
| C.依据沸点的数据,判断用分馏的方法从石油中获取汽油和煤油等 |
| D.依据燃烧热的数据、热化学方程式和盖斯定律,可计算一些反应的反应热 |
下列说法不正确的是
| A.钠与乙醇反应,钠块沉在乙醇液面下面 |
| B.除去乙酸乙酯中残留的乙酸,可用饱和Na2CO3溶液洗涤后分液 |
| C.伴有能量变化的物质变化都是化学变化 |
| D.化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+ O2(g)=SO2(g)+H2O(g) △H1
②2H2S(g)+SO2(g)=S2 (g)+2H2O(g) △H2
③H2S(g)+O2(g)=S(g)+H2O(g) △H3
④ 2S(g) =S2(g) △H4
则△H4的正确表达式为
| A.△H4=(△H1+△H2-3△H3) | B.△H4=(3△H3-△H1-△H2) |
| C.△H4=(△H1+△H2-3△H3) | D.△H4=(△H1-△H2-3△H3) |
参照反应Br+H2→HBr+H的能量随反应历程变化的示意图,下列叙述中正确的是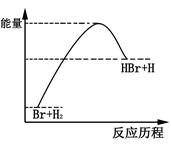
| A.正反应为吸热反应 |
| B.该反应的逆反应是吸热过程 |
| C.HBr的能量一定高于H2的能量 |
| D.反应物具有的总能量大于生成物具有的总能量 |
同温同压下,已知下列各反应均为放热反应,其中放热最少的是( )
| A.2A ( l ) + B ( l ) =" 2C" ( g ) ΔH1 | B.2A ( g ) + B ( g ) =" 2C" ( g ) ΔH2 |
| C.2A ( g ) + B ( g ) =" 2C" ( l ) ΔH3 | D.2A ( l ) + B ( l ) =" 2C" ( l ) ΔH4 |