下列化合物,按其晶体的熔点由高到低排列正确的是
| A.SiO2 CaCl2 CBr4CF4 | B.SiO2CsCl CF4CBr4 |
| C.CsCl SiO2 CBr4CF4 | D.CF4CBr4CsCl SiO2 |
下列对各组物质性质的比较中,正确的是
| A.第一电离能:Na<Mg<Al |
| B.熔点:金刚石>晶体硅>碳化硅 |
| C.硬度:Li>Na>K |
| D.空间利用率:六方密堆<面心立方<体心立方 |
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700oC时反应制造出 纳米级金刚石粉末和另一种化合物。该成果发表在世界权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些“理解”,你认为其中错误的是:
| A.这个反应是氧化还原反应 | B.制造过程中元素种类没有改变 |
| C.另一种化合物为NaCl | D.金刚石属于金属单质 |
石墨烯是由碳原子构成具有片状结构的新型纳米材料(结构示意图如下),可通过剥离石墨而成,具有极好的应用前景。下列说法正确的是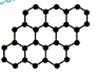
| A.石墨烯是一种有机化合物 |
| B.0.0012kg石墨烯中含有0.6mol质子 |
| C.不用其它试剂,利用丁达尔现象即可区分石墨和石墨烯 |
| D.剥离石墨属于物理变化过程 |
有关晶体的下列说法中正确的是
| A.晶体中分子间作用力越大,分子越稳定 |
| B.原子晶体中共价键越强,熔点越高 |
| C.冰熔化时水分子中共价键发生断裂 |
| D.氯化钠熔化时离子键未被破坏 |
下列有关说法正确的是( )
| A.乙醇与浓硫酸170℃共热,制得的气体直接通入溴水,可检验制得的气体是否为乙烯 |
| B.合成氨工业中,利用氨易液化,分离出N2、H2循环使用,可提高氨的产率 |
| C.将(NH4)2Fe(SO4)2·6H2O溶于稀硝酸,滴加KSCN溶液出现血红色,说明试样已变质 |
| D.由ⅠA族和ⅦA族的元素形成的离子晶体,晶体的结构完全相同 |
最近科学家成功制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体叙述错误的是
| A.该晶体类型是原子晶体 |
| B.晶体中碳原子数与C—O化学键数之比为1∶2 |
| C.晶体的空间最小环共有12个原子构成 |
| D.该晶体中碳原子和氧原子的个数比为1∶2 |
已知X、Y、Z三种元素组成的化合物是离子晶体,其晶胞如图所示,则下面表示该化合物的化学式正确的的是
| A.ZXY3 | B.ZX2Y6 | C.ZX4Y8 | D.ZX8Y12 |
“拟晶”(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质。A165Cu23Fel2是二十世纪发现的几百种拟晶之一,具有合金的某些优良物理性能。有关这种拟晶的说法错误的是:
| A.A165Cu23Fel2的硬度比金属A1、Cu、Fe都大 |
| B.A165Cu23Fel2中三种金属的化合价均可视作零 |
| C.A165Cu23Fel2不可用作长期浸泡在海水中的材料 |
| D.1mol A165Cu23Fel2溶于过量的硝酸时共失去265 mol电子 |
下列叙述正确的是( )
| A.原子晶体中,共价键的键能越大,熔沸点越高 |
| B.分子晶体中,分子间作用力越大,该分子越稳定 |
| C.分子晶体中,共价键键能越大,熔沸点越高 |
| D.某晶体溶于水中,可电离出自由移动的离子,该晶体一定是离子晶体 |