题目内容
下列有关说法正确的是( )
| A.乙醇与浓硫酸170℃共热,制得的气体直接通入溴水,可检验制得的气体是否为乙烯 |
| B.合成氨工业中,利用氨易液化,分离出N2、H2循环使用,可提高氨的产率 |
| C.将(NH4)2Fe(SO4)2·6H2O溶于稀硝酸,滴加KSCN溶液出现血红色,说明试样已变质 |
| D.由ⅠA族和ⅦA族的元素形成的离子晶体,晶体的结构完全相同 |
B
解析试题分析:制备乙烯时容易产生副产物气体SO2等还原气体使溴水褪色,所以应该先通过碱性洗气瓶,A错误;利用化学平衡原理,减小生成物的浓度、增大反应物的浓度可以使平衡向正反应移动,提高氨的产率,B正确;用硝酸溶解(NH4)2Fe(SO4)2·6H2O,容易把亚铁离子氧化为铁离子,所以滴加KSCN试剂必然显红色,不能说明变质,C错误;由ⅠA族和ⅦA族的元素形成的离子晶体的结构部完全相同,D错误;故选B。
考点:本题考查的是有机实验、化学平衡、离子检验、晶体等基础知识。

练习册系列答案
相关题目
下列各组物质中,按熔点由低到高排列正确的是( )
| A.O2、I2、Hg | B.CO2、KCl、SiO2 |
| C.HF、HCl、HI | D.SiO2、NaCl、SO2 |
金属晶体的形成是因为晶体中主要存在 ( )
| A.金属离子之间的相互作用 | B.金属原子之间的作用 |
| C.金属离子与自由电子间的相互作用 | D.金属原子与自由电子间的相互作用 |
下列化合物,按其晶体的熔点由高到低排列正确的是
| A.SiO2 CaCl2 CBr4CF4 | B.SiO2CsCl CF4CBr4 |
| C.CsCl SiO2 CBr4CF4 | D.CF4CBr4CsCl SiO2 |
关于晶体的叙述中,正确的是
| A.原子晶体中,共价键的键能越大,熔、沸点越高 |
| B.分子晶体中,分子间的作用力越大,该分子越稳定 |
| C.分子晶体中,共价键的键能越大,熔、沸点越高 |
| D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体 |
某化学式为AB的离子晶体,已知5r(A2+)=4r(B2-)(各类离子晶体与 关系如下图所示),经测定其密度为
关系如下图所示),经测定其密度为 g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
| r+/r- | 配位数 | 实例 |
| 0.225~0.414 | 4 | ZnS |
| 0.414~0.732 | 6 | NaCl |
| 0.732~1.0 | 8 | CsCl |
| >1.0 | 12 | CsF |
A.该晶体结构与ZnS晶体相似
B.该晶体每个晶胞中有2个A2+和B2-
C.该晶体晶胞的边长为
 cm
cmD.A2+离子紧邻的B2-构成的空间结构为立方体
已知反应A+B=C+D的能量变化如右图所示,下列说法正确的是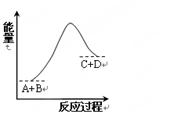
| A.该反应为放热反应 |
| B.该反应为吸热反应 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应只有在加热条件下才能进行 |
下列说法正确的是
| A.7.8克Na2S和Na2O2的固体混合物中含有的阴离子数目为0.1NA |
B.用铜做电极电解CuSO4溶液的反应方程式: 2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| C.常温时,浓度均为0.01mol/L的 Na2CO3溶液和NaHCO3溶液等体积混合,其溶液中粒子浓度关系为c(CO32-) +c(HCO3-)+c(H2CO3) =0.02mol/L |
| D.在蒸馏水中滴加浓H2SO4,KW不变 |